理化学研究所(理研)開拓研究所 眞貝細胞記憶研究室の島津 忠広 専任研究員、眞貝 洋一 主任研究員らの研究グループは、METTL18[1]という酵素がマウスで膵臓(すいぞう)の正常な働きを支える重要な役割を担っていることを明らかにしました。
本研究成果は、膵臓の病気の仕組みの解明につながることが期待されます。
タンパク質は細胞内で正しくつくられ、適切な状態に保たれることで機能します。その過程にはさまざまな化学修飾が関わります。島津専任研究員らは以前、METTL18がリボソームの構成要素のヒスチジン(His)残基をメチル化修飾し、タンパク質合成の進み方を調節していることを明らかにしました。今回、研究グループは、METTL18を欠損させたマウスでは膵臓でタンパク質の異常な蓄積が起こり、低体重、高血糖、低インスリンなどの糖尿病様の症状を示すことを発見しました。膵臓由来細胞を用いた実験から、METTL18を欠くとタンパク質が適切に折り畳まれず凝集して小胞体ストレス応答[2]と炎症反応[3]が起きることも分かりました。これが原因で、膵臓の機能障害が起こると考えられます。本研究は、METTL18によるHisメチル化修飾が膵臓で重要な役割を担うことを明確に示した成果です。
本研究は、科学雑誌『Molecular Metabolism』(2026年4月号)の掲載に先立ち、オンライン版(2月27日付)に掲載されました。
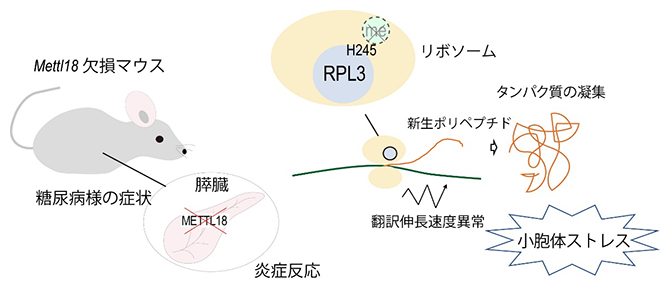
METTL18欠損マウスにおける膵臓機能障害
背景
細胞内で翻訳されたタンパク質は、その後、さまざまな種類の化学的な修飾を受けます。このような化学修飾を「翻訳後修飾」と呼び、タンパク質の構造や細胞内局在、酵素活性、他の分子との相互作用など、タンパク質の機能を決める上で非常に重要な役割を果たします。
島津専任研究員らは以前、METTL18という酵素が、リボソームタンパク質RPL3[4]の特定のヒスチジン(His)残基(H245)をメチル化修飾することで、翻訳伸長におけるコドン(タンパク質のアミノ酸の並び方の情報)の読み取り速度を適切に保っていることを見いだしました注)。この研究は細胞レベルでのHis残基メチル化の生理的意義を明らかにしましたが、同修飾が生体内ではどのような意義を持つのかは不明でした。今回、研究グループではMETTL18を欠損したマウスを作出し、欠損マウスがどのような症状を示すのか、解析しました。
- 注)2022年6月21日プレスリリース「リボソームタンパク質に起きる翻訳後修飾の機能」
研究手法と成果
CRISPR-Cas9[5]を用いたゲノム編集技術によってMettl18遺伝子を欠損した(KO)マウスを作出し、野生型(WT)マウスと比較することで主な組織のRPL3メチル化を評価しました。その結果、RPL3のHisメチル化は特にWTマウスの膵臓で顕著に見られる一方で、KOマウスではメチル化が起こらないことが分かりました(図1A)。
Mettl18 KOマウスの一部は胎生致死となること、出生したKOマウスも生育不全があることが分かりました。膵臓は、インスリンを分泌し血糖値の調節をする働きがあることから、KOマウスの血清グルコース濃度や血清インスリン濃度を測定したところ、KOマウスはWTマウスに比べて高グルコース(図1B)、低インスリン(図1C)であることが判明しました。さらに、経口グルコース負荷試験を行ったところ、KOマウスでは耐糖能の低下が見られたことから、Mettl18 KOマウスではRPL3のHisメチル化が消失し、糖尿病様の症状を示すことが分かりました(図1D)。このことは、Mettl18が膵臓において、血糖値の恒常性維持に重要であることを示しています。
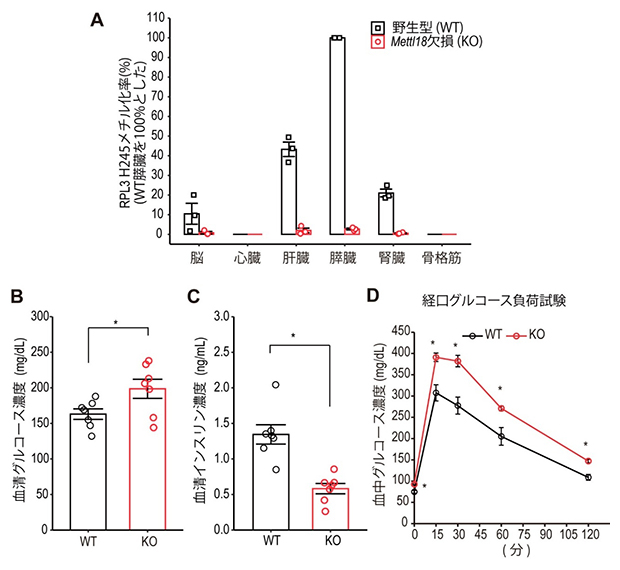
図1 Mettl18の膵臓機能(血糖値の恒常性維持)への重要性
- (A)野生型(WT)とMettl18欠損(KO)マウスの主要な臓器でのRPL3H245メチル化状態。各組織におけるメチル化率は、抗RPL3抗体およびRPL3のH245メチル化修飾を特異的に認識する抗体でウエスタンブロット(タンパク質検出法)を行い、定量することで算出した。
- (B)自由給餌条件での血清中のグルコース濃度。
- (C)自由給餌条件での血清中のインスリン濃度。
- (D)経口グルコース負荷試験。24時間絶食したマウスにグルコース(2g/kg体重)を経口投与した後、血糖値を経時的に測定した。
「*」は、有意差があることを示す。
島津専任研究員らは以前、METTL18がリボソームタンパク質RPL3のメチル化を行うことでタンパク質合成の伸長を調節すること、KO細胞ではタンパク質の凝集が起きることを見いだしており注)、今回、KOマウスの膵臓でもタンパク質の凝集が起きているのかを検討しました。その結果、Mettl18を欠損した膵臓由来細胞では膵石(すいせき)タンパク質Reg1[6]などの蓄積が見られること(図2A、2B)、マウス膵臓組織では小胞体ストレス応答と炎症性サイトカイン(細胞外に分泌される情報伝達物質のタンパク質)の発現上昇が起きていることが分かりました(図2C)。このことは、Mettl18が膵臓でのタンパク質合成と恒常性の維持に重要であることを示しています。
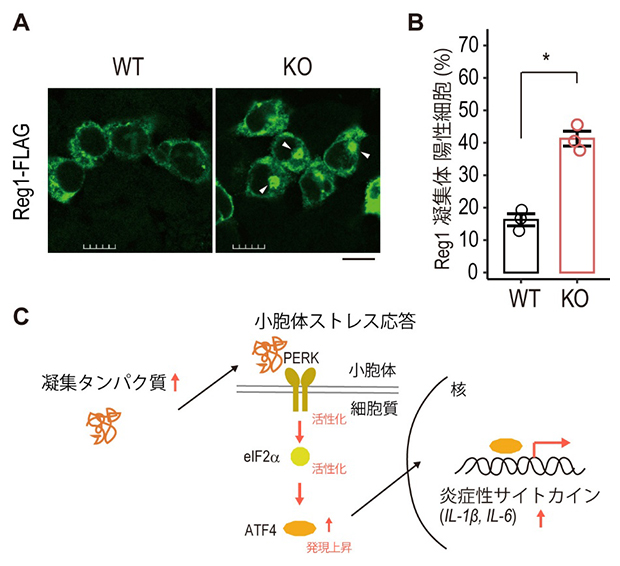
図2 Mettl18のない細胞におけるタンパク質凝集と小胞体ストレス応答
- (A)マウスの膵臓にある腺房細胞の株(266-6細胞)にFLAGタグを付加したReg1(Reg1-FLAG)を発現させ、2日後に免疫染色法により蛍光顕微鏡観察を行った。KO細胞の白矢頭は、凝集体を示す。スケールバーは10マイクロメートル(μm、1μmは100万分の1メートル)を表す。
- (B)凝集体陽性細胞の割合(パーセンテージ)をカウントした。「*」は、有意差があることを示す。
- (C)Mettl18 KOマウスの膵臓では、小胞体ストレス応答(PERK(PKR-like endoplasmic reticulum kinase)やeIF2α(翻訳開始因子α)の活性化とATF4(Activating Transcription Factor 4)の発現上昇)と炎症性サイトカイン(IL-1β、IL-6)の発現上昇が起こる。
KO細胞での翻訳異常を詳しく調べるために、コドン読み取り速度(伸長速度)を調べたところ、METTL18がない膵臓由来細胞では、野生型細胞と比べてコドンごとの伸長速度に変化が見られました(図3A)。特に、KO細胞ではアミノ酸の一種であるプロリンをコードするコドンの伸長速度が速くなっていることが分かりました。さらに、プロリンの含有量が多いタンパク質(Prh1、プロリンを42モルパーセント(mol%)含有)はKO細胞で凝集を形成したことから(図3B、3C)、プロリンコドンの読み取りの速さの違いがタンパク質凝集につながっている可能性が考えられました。
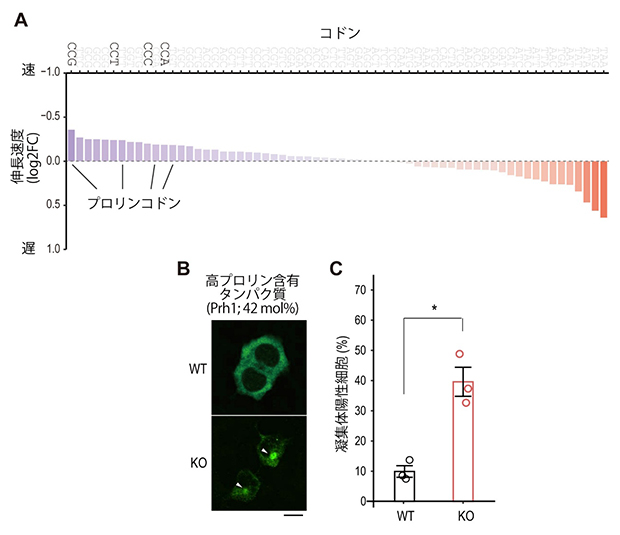
図3 Mettl18によるコドンの読み取り速度の適切な調節
- (A)Mettl18 KO 266-6細胞でのコドン読み取り速度の変化。WT細胞と比較してKO細胞で伸長速度が速いコドンほど、log2FC(コドンの占有率)の値が小さくなる。
- (B)Mettl18 KO 266-6細胞にFLAGタグを付加した高プロリン含有タンパク質(Prh1-FLAG)を細胞に発現させ、2日後に免疫染色法により蛍光顕微鏡観察を行った。KO細胞の白矢頭は、凝集体を示す。スケールバーは10μmを表す。
- (C)凝集体陽性細胞の割合(パーセンテージ)をカウントした。「*」は、有意差があることを示す。
今後の期待
本研究は、METTL18によるヒスチジン(His)修飾が膵臓においてタンパク質合成の正確性と品質維持に重要であることを示しました。本成果は、ヒスチジン修飾を代謝恒常性制御の新たな調節機構として位置付ける基盤となるものです。
今後、ヒスチジン修飾の異常が糖尿病や代謝疾患の発症にどの程度関与しているのかを明らかにする必要があるとともに、METTL18の機能低下が小胞体ストレスやインスリン分泌異常を引き起こす、より詳細な分子機構の解明も課題です。このような研究が進み、ヒスチジン修飾を制御する因子や関連経路が分かれば、新たな病態の理解につながることが期待できます。将来的には、METTL18や関連分子を標的とした糖尿病や代謝疾患の診断・治療戦略の開発も期待されます。
補足説明
- 1.METTL18
7βストランド型のメチル化酵素ドメインを持ち、ヒトから酵母まで真核生物に広く保存されている。2010年に酵母のHPM1(ヒトMETTL18のホモログ)がRPL3([4]参照)のヒスチジン(His)残基をメチル化することが報告され、その後2021年から2022年にかけて、島津専任研究員らのグループを含めた複数の研究グループからヒトMETTL18がRPL3のヒスチジン残基をメチル化することが報告された。 - 2.小胞体ストレス応答
細胞内の小胞体で異常タンパク質が蓄積(小胞体ストレス)した際、それを感知して修正・除去する生体防御機構。 - 3.炎症反応
小胞体ストレス応答が慢性化するとインフラマソーム(炎症小体)を活性化し、IL-1βやTNF-αなどの炎症性サイトカインを放出させ、慢性炎症や糖尿病、神経変性疾患などを誘発することが知られる。 - 4.RPL3
リボソームは細胞内のタンパク質合成を担う大きなリボ核タンパク質複合体であり、RPL3はリボソームの大サブユニットの構成ユニットの一つである。 - 5.CRISPR-Cas9
標的ゲノム領域を認識する配列とCas9と複合体を形成する配列から成るgRNA(ガイドRNA)およびヌクレアーゼ活性によりDNAを切断するCas9タンパク質から成る。これらを細胞や受精卵に導入すると、複合体を形成して標的ゲノムを切断する。細胞がこれを修復する際の複製エラーにより、ゲノムに欠失や挿入が起きる。また、切断部位に相同組換えなどにより外来遺伝子をノックインできる。 - 6.Reg1
膵石タンパク質(Pancreatic Stone Protein、PSP/PSPS1)やリトスタチン(Lithostathin)とも呼ばれるタンパク質で、主に膵臓で産生され、膵臓の再生・機能維持に関与している可能性が示唆されている。また、慢性膵炎では、膵石の主な構成成分であることが知られる。
研究グループ
理化学研究所
開拓研究所
眞貝細胞記憶研究室
専任研究員 島津 忠広(シマヅ・タダヒロ)
研修生(研究当時)五輪 愛未(ゴワ・メグミ)
テクニカルスタッフⅡ 片岡 礼音(カタオカ・アヤネ)
主任研究員 眞貝 洋一(シンカイ・ヨウイチ)
岩崎RNAシステム生化学研究室
上級研究員(研究当時)七野 悠一(シチノ・ユウイチ)
(現 客員研究員、筑波大学 医学医療系 教授)
大学院生リサーチ・アソシエイト 戸室 幸太郎(トムロ・コウタロウ)
主任研究員 岩崎 信太郎(イワサキ・シンタロウ)
環境資源科学研究センター
生命分子解析ユニット
専任技師 鈴木 健裕(スズキ・タケヒロ)
ユニットリーダー 堂前 直(ドウマエ・ナオシ)
研究支援
本研究は、理研横断プロジェクト「エピゲノム操作(研究代表者:眞貝洋一)」、日本学術振興会(JSPS)科学研究費助成事業学術変革領域研究(B)「neo-PTMsの生命機能解析(研究代表者:島津忠広、JP22H05020)」、武田科学振興財団「ビジョナリーリサーチ継続助成(ホップ)(研究代表者:島津忠広)」による助成を受けて行われました。
原論文情報
- Tadahiro Shimazu, Megumi Gowa, Ayane Kataoka, Takehiro Suzuki, Kotaro Tomuro, Yuichi Shichino, Naoshi Dohmae, Shintaro Iwasaki, Yoichi Shinkai, "METTL18 Ensures Pancreatic Function by Maintaining Proper Translation and Proteostasis", Molecular Metabolism, 10.1016/j.molmet.2026.102337
発表者
理化学研究所
開拓研究所 眞貝細胞記憶研究室
専任研究員 島津 忠広(シマヅ・タダヒロ)
主任研究員 眞貝 洋一(シンカイ・ヨウイチ)
 島津 忠広
島津 忠広
 眞貝 洋一
眞貝 洋一
報道担当
理化学研究所 広報部 報道担当
お問い合わせフォーム
