理化学研究所(理研)生命医科学研究センター 空間免疫制御理研ECL研究ユニットの佐藤 尚子 理研ECL研究ユニットリーダー(開拓研究所 佐藤空間免疫制御理研ECL研究ユニット 理研ECL研究ユニットリーダー)、粘膜システム研究チームの長田 律 リサーチアソシエイト、大野 博司 チームディレクターらの国際共同研究グループは、腹膜炎[1]発症時における内臓脂肪組織を介する免疫制御機構の一端を明らかにしました。
今回、国際共同研究グループは、消化管穿孔(しょうかかんせんこう)により腹膜炎を発症させたマウスの内臓脂肪組織を解析し、免疫細胞の自然リンパ球(ILC)[2]の一種である1型自然リンパ球(ILC1)が過剰な炎症を抑制することで腹膜炎の収束に重要な役割を果たすことを突き止めました。本研究成果は、急性炎症時における内臓脂肪組織の免疫学的役割の理解につながると期待されます。
本研究は、科学雑誌『Nature Communications』オンライン版(3月12日付)に掲載されました。
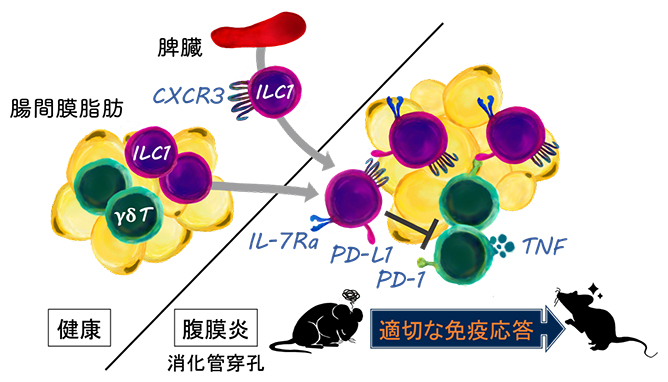
腹膜炎発症時の過剰な炎症を負に調節する脂肪組織内ILC1
背景
腹膜炎は消化管穿孔により胃や腸の内容物が腹腔内(ふくくうない)に漏出することで引き起こされる急性炎症であり、死亡率の高い敗血症[3]に病態移行する場合があるため、炎症早期の適切な処置が生存率の向上に必須です。
内臓脂肪組織は、肥大すると代謝疾患を促進するなど、身近にその存在が認知されている生体組織です。ただ、興味深いことに、内臓脂肪組織には多種の免疫細胞が存在し、免疫応答器官としての役割も有しています。しかしながら、腹膜炎などの急性炎症時における内臓脂肪組織の免疫学的役割はほとんど知られていませんでした。
研究手法と成果
国際共同研究グループは、腹膜炎モデルマウスを用いた解析により、これまで腹膜炎や敗血症の研究で着目されていなかった、免疫細胞の一種である1型自然リンパ球(ILC1)が消化管穿孔時の内臓脂肪組織内の過剰な炎症を抑制するというユニークな免疫制御機構を明らかにしました。具体的な内容は次の通りです。
まず、腹膜炎を誘導したマウスの病態を測定しました。サイトカイン[4]の一種で炎症マーカーのインターロイキン-6(IL-6)の産生量を血中と脂肪組織で調べた結果、IL-6の産生量は腹膜炎誘導6時間後に増加し、24時間後までに腹膜炎誘導前と同程度までに減少しました(図1A)。したがって、腹膜炎マウスの病態は敗血症に移行せずに回復することが分かりました。次に腹膜炎マウスの脂肪組織内の免疫細胞を解析した結果、炎症が亢進(こうしん)する腹膜炎誘導6時間後に自然リンパ球(ILC)の一種であるILC1が増加していました(図1B)。また、腹膜炎発症時にILC1が脾臓(ひぞう)から脂肪組織へ移動していることも分かりました。
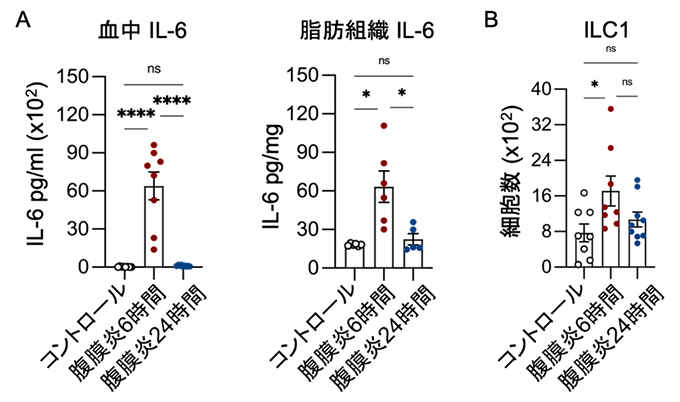
図1 腹膜炎マウスの病態経時変化の解析
- A.血中および脂肪組織内のIL-6の産生量は腹膜炎誘導6時間後に増加した。
- B.炎症時の脂肪組織内でILC1が増加した。pg:ピコ(1兆分の1)グラム。
統計的有意差: *P<0.05、****P<0.0001。ns:「not significant(有意差なし)」の略号。
次に、増加したILC1の詳細な解析を行いました。これまでの報告から健常時の脂肪組織では、ILC1は、自然リンパ球の細胞表面マーカーの一つであるCD127(インターロイキン-7の受容体)を発現しないことが知られています。実際に腹膜炎を誘導していないコントロール(対照群)マウスの脂肪組織ではILC1はCD127を発現していませんでしたが、腹膜炎を誘導したマウスではCD127を発現するILC1が増加しました(図2A)。さらにILC1は感染時に炎症促進因子であるインターフェロン(IFN)-γを産生することが知られているため、CD127陰性および陽性ILC1におけるIFN-γ産生能を測定しました。興味深いことに、CD127陽性ILC1のIFN-γ産生能は腹膜炎誘導後においても低いことが分かりました(図2B)。以上より、腹膜炎発症時の内臓脂肪組織で増加したILC1はこれまでの報告とは異なる特徴を有することが明らかとなりました。
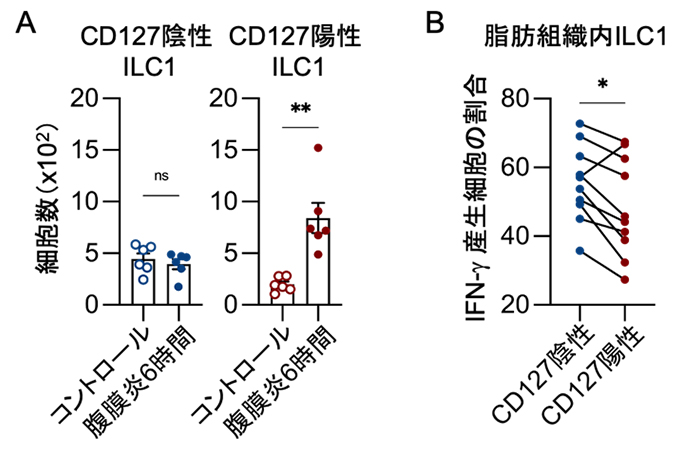
図2 腹膜炎マウスの脂肪組織で増加するCD127陽性ILC1の解析
- A.腹膜炎誘導6時間後の脂肪組織でCD127陽性ILC1が増加した。
- B.腹膜炎誘導6時間後の脂肪組織では、CD127陽性(赤)ILC1内のIFN-γ産生細胞の割合はCD127陰性(青)ILC1より少なかった。
統計的有意差: *p<0.05、**p<0.01。ns:「not significant(有意差なし)」の略号。
次に国際共同研究グループは、このユニークなILC1がどのように腹膜炎の病態制御に関与しているのかについて解析を試みました。CD127陽性ILC1に特徴的な遺伝子発現およびタンパク質発現を解析した結果、免疫抑制因子であるPD-L1[5]が検出されました(図3A)。PD-L1は免疫細胞であるT細胞[6]に発現するPD-1[5]に作用して、T細胞の活性を抑制する機能があります。そこで脂肪組織内の各種T細胞のPD-1発現を調べた結果、腹膜炎誘導6時間後のγδT細胞[7]でPD-1の顕著な発現上昇が認められました(図3B)。さらにPD-1の機能を阻害すると、腹膜炎発症時のγδT細胞では炎症促進因子であるTNFの産生が増加していました(図3C)。以上より、腹膜炎発症時の脂肪組織内CD127陽性ILC1はPD-L1を介してγδT細胞の活性を抑制している可能性が示唆されました。
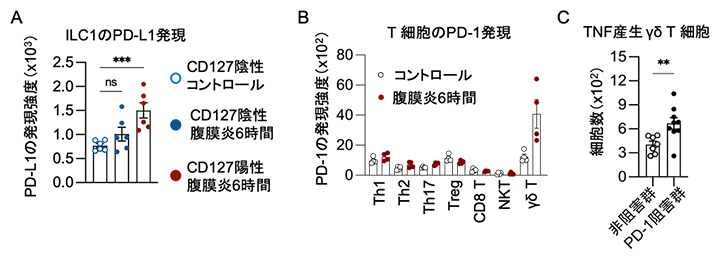
図3 腹膜炎マウスの脂肪組織内PD-1陽性γδT細胞の解析
- A.腹膜炎誘導6時間後の脂肪組織でCD127陽性ILC1のPD-L1発現量が増加した。
- B.腹膜炎誘導6時間後の脂肪組織でγδT細胞のPD-1発現量が増加した。
- C.PD-1の機能阻害により、腹膜炎誘導6時間後の脂肪組織では、TNFを産生するγδT細胞が増加した。
統計的有意差: *p<0.05、**p<0.01、***p<0.001。ns:「not significant(有意差なし)」の略号。
ILC1がγδT細胞に及ぼす影響をさらに調べるため、ILC1欠損マウスを用いた解析を行いました。野生型マウスおよびILC1欠損マウスに腹膜炎を誘導した結果、ILC1欠損マウスでは炎症マーカーの発現増加とともに、生存率の低下が見られました(図4A)。さらに、脂肪組織内のγδT細胞を解析した結果、ILC1欠損マウスのγδT細胞ではPD-1発現が低下し、TNF産生能は増加しました(図4B)。また、ILC1欠損マウスにTNF阻害剤を投与すると病態の改善が見られました(図4C)。
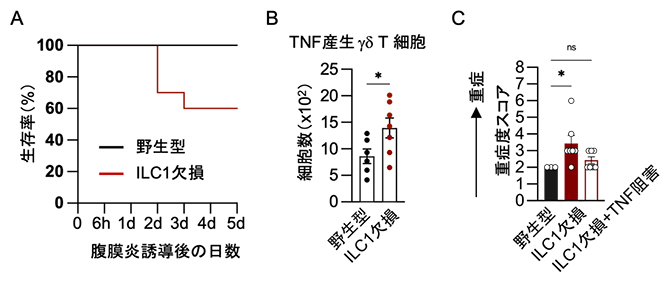
図4 ILC1の欠損が腹膜炎マウスに与える影響の解析
- A.ILC1の欠損により腹膜炎誘導後の病態が悪化した。
- B.ILC1の欠損により、腹膜炎誘導6時間後の脂肪組織でTNF産生γδT細胞が増加した。
- C.ILC1欠損マウスにTNF阻害剤を投与すると病態の改善が認められた。
統計的有意差: *p<0.05。ns:「not significant(有意差なし)」の略号。
以上より、脂肪組織においてILC1がγδT細胞を介して過剰な炎症を抑制することで腹膜炎の収束に重要な役割を担っている可能性が明らかとなりました。
今後の期待
本研究により、腹膜炎発症時に内臓脂肪組織が免疫器官としても機能することが明らかとなり、早期治療ターゲットとしての内臓脂肪組織の重要性が示されました。しかしながら、脂肪組織内の免疫細胞の組成や性質はヒトとマウスで異なることが知られており、今後は、ヒトのサンプルでの解析が必要とされています。
補足説明
- 1.腹膜炎
腹腔内の内臓を覆う膜である腹膜に炎症が生じた症状。虫垂炎や大腸がんなどにより消化管穿孔が生じると腸内細菌が無菌状態の腹腔内に漏出し、急性で強い炎症状態を呈する腹膜炎が引き起こされる。 - 2.自然リンパ球(ILC)
T細胞([6]参照)やB細胞と類似した形態的特徴を有するが、T細胞受容体やB細胞受容体を発現しない。大きく五つのサブセットILC1、ILC2、ILC3、NK細胞およびLTi細胞に分けられ、サブセットそれぞれが特徴的なサイトカイン([4]参照)を産生し、種々の生体反応に関与する。ILCはinnate lymphoid cellsの略。 - 3.敗血症
感染による宿主生体反応の制御不全により他臓器機能不全を呈した病態。死亡率が高い。 - 4.サイトカイン
免疫細胞や実質細胞などから産生され、免疫細胞の活性化や抑制化を誘導することで炎症を引き起こし、調節する液性因子。炎症を促進するものは炎症性サイトカインと呼ばれ、IL-6、IFN-γ、TNFなどが知られている。一方で炎症を抑制するものは抑制性サイトカインと呼ばれIL-10やTGF-βなどが知られている。 - 5.PD-L1、PD-1
PD-1は主に活性化したT細胞([6]参照)に発現する抑制性受容体であり、結合相手であるPD-L1が結合すると、T細胞の増殖やサイトカイン([4]参照)産生などが低下する。 - 6.T細胞
それぞれが異なる異物を認識する免疫細胞集団であり、サイトカイン産生や細胞障害活性などを介して免疫応答に関与する。 - 7.γδT細胞
生体内T細胞の大部分を占める、細胞表面の受容体がα(アルファ)鎖とβ(ベータ)鎖の2本鎖にて構成されているαβT細胞とは異なり、γ(ガンマ)鎖およびδ(デルタ)鎖から成る。皮膚、腸管上皮、脂肪組織など非リンパ組織に高い割合で存在する。炎症時には迅速にサイトカイン産生や細胞傷害活性を介して主に炎症初期~中期の免疫応答に関与する。
国際共同研究グループ
理化学研究所 生命医科学研究センター
空間免疫制御理研ECL研究ユニット
理研ECL研究ユニットリーダー 佐藤 尚子(サトウ・ナオコ)
(開拓研究所 佐藤空間免疫制御理研ECL研究ユニット 理研ECL研究ユニットリーダー)
テクニカルスタッフⅠ 影山 友子(カゲヤマ・トモコ)
粘膜システム研究チーム
チームディレクター 大野 博司(オオノ・ヒロシ)
リサーチアソシエイト 長田 律(ナガタ・リツ)
テクニカルスタッフⅡ 川住 雅美(カワスミ・マサミ)
研修生(研究当時)佐藤 真那美(サトウ・マナミ)
三重大学 大学院医学系研究科 分子病態学研究室
教授 島岡 要(シマオカ・モトム)
ファインスタイン医学研究所(米国)
研究員 赤間 悠一(アカマ・ユウイチ)
パスツール研究所(フランス)自然免疫ユニット
博士研究員 ペドロ・ゴンカルベス(Pedro Goncalves)
研究員 ニコラス・セラフィニ(Nicolas Serafini)
研究支援
本研究は、日本学術振興会(JSPS)科学研究費助成事業国際共同研究加速基金国際共同研究強化(A)(研究代表者:佐藤尚子、JP20KK0360)、日本医療研究開発機構(AMED)革新的先端研究開発支援事業(研究代表者:佐藤尚子、JP21gm6310027h)、同ムーンショット型研究開発事業(研究分担者:大野博司、JP22zf0127007)、公益財団法人臨床薬理研究振興財団(研究代表者:佐藤尚子)による助成を受けて行われました。
原論文情報
- Ritsu Nagata, Yuichi Akama, Pedro Goncalves, Nicolas Serafini, Tomoko Kageyama, Masami Kawasumi, Manami Satoh, Motomu Shimaoka, Hiroshi Ohno* and Naoko Satoh-Takayama*(* は共同責任著者), "Acute peritonitis-induced adipose CD127+ ILC1s express PD-L1 and ameliorate inflammation in mice", Nature Communications, 10.1038/s41467-026-69100-0
発表者
理化学研究所
生命医科学研究センター
空間免疫制御理研ECL研究ユニット
理研ECL研究ユニットリーダー 佐藤尚子(サトウ・ナオコ)
(開拓研究所 佐藤空間免疫制御理研ECL研究ユニット 理研ECL研究ユニットリーダー)
粘膜システム研究チーム
チームディレクター 大野 博司(オオノ・ヒロシ)
リサーチアソシエイト 長田 律(ナガタ・リツ)
 佐藤 尚子
佐藤 尚子
 大野 博司
大野 博司
 長田 律
長田 律
報道担当
理化学研究所 広報部 報道担当
お問い合わせフォーム
