理化学研究所(理研)環境資源科学研究センター 細胞機能研究チームの岩瀬 哲 上級研究員、杉本 慶子 チームディレクターらの共同研究グループは、植物が傷付いたときなどに組織を再生させる能力のスイッチとして働くWIND1という転写因子[1]が、将来どのような細胞や組織になるかという発生運命[2]を転換する制御原理を発見しました。
本研究成果は、組織培養技術を用いた増産や品種改良など、植物による持続的な食料や有用物質の生産、新規の遺伝子発現制御法の開発に貢献するものです。
植物の再生を促す重要な転写因子は複数知られていますが、単独の転写因子がどのように発生運命を転換させるのか、その詳しい分子メカニズムは分かっていませんでした。一方、転写因子WIND1は、傷害ストレスによるカルス[3]形成や、茎葉(けいよう:植物の茎や葉)などの再生、さらには道管[4]の再形成や、病原体の感染を防ぐ防御応答などを促進することが分かっています。
今回、共同研究グループは、WIND1によって体細胞胚(不定胚)[5]が効率的に誘導される実験系をまず開発しました。この実験系を用いてアブラナ科のモデル植物、シロイヌナズナがWIND1によってどのように発生運命を、茎葉から体細胞胚に転換するのか調べました。この結果、WIND1がヒストンのアセチル化と脱アセチル化[6]という相反するエピジェネティック修飾[7]の両方を制御することを明らかにしました。この制御を介してWIND1はもともと芽生えが有していた茎葉の発生運命を遺伝子発現レベルで抑制しつつ、体細胞胚になる新たな発生運命の獲得に必要な重要遺伝子群の発現を促進していることが分かりました。
本研究は、科学雑誌『Molecular Plant』オンライン版(3月10日付)に掲載されました。
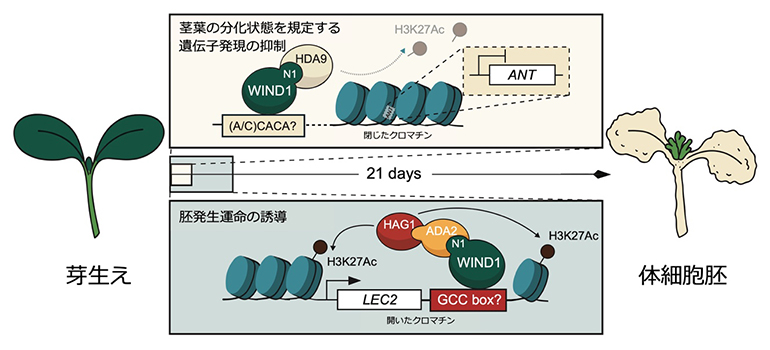
WIND1はヒストン修飾複合体を形成し、遺伝子発現のオン/オフを切り替えて発生運命を転換
背景
植物は高い再生能力を持つことが古くから知られており、その再生能力は接ぎ木や挿し木などの方法で現在でも農業や園芸分野で広く利用されています。プラナリアやイモリなどの動物にも高い再生能力を示す例は存在しますが、分化した体細胞から胚発生プログラムを再起動し、体細胞胚を形成できる再生能力は植物で特に顕著です。この体細胞胚の形成は、植物細胞が有する全ての細胞種に分化できる潜在能力である分化可塑性(分化全能性)を示す代表的な現象として知られています。
岩瀬上級研究員らは、これまで植物が種々のストレスに応じて組織再生を引き起こすメカニズムについて解析を進め、2011年にシロイヌナズナで傷口の細胞の脱分化を促進する転写因子WIND1(WOUND INDUCED DEDIFFERENTIATION1)や同じ機能を持つWIND2~4を発見しました注1)。さらに分化した細胞ではWIND転写因子群の働きをエピジェネティック[7]に抑える機構があること注2)、WIND1がESR1という別の転写因子の働きを傷口で活性化させることによって傷口のカルス形成や茎葉の再生を促進していること注3)、またWIND1が再生のみならず、傷害ストレス後の道管形成や防御応答を活性化していること注4)を明らかにしてきました。
今回、共同研究グループはシロイヌナズナを用いて、WIND1転写因子を発現させるだけで芽生えから体細胞胚を効率的に誘導する実験システムを構築し、WIND1がどのように茎葉から体細胞胚に発生運命を切り替えているのか調べました。
- 注1)2011年3月11日プレスリリース「植物細胞の脱分化を促進するスイッチ因子を発見」
- 注2)2015年6月30日プレスリリース「植物の分化全能性抑制の分子メカニズムの一端を解明」
- 注3)2017年1月17日プレスリリース「植物が傷口で茎葉を再生させる仕組み」
- 注4)2021年8月20日プレスリリース「植物の再生と防御のスイッチ」
研究手法と成果
実験には、WIND1遺伝子を人為的に発現誘導できるシロイヌナズナのXVE-WIND1植物体を用いました。液体培地の中で芽生えさせた5日齢のXVE-WIND1植物体でWIND1を発現させ、そのまま培養を続けると、添加後14日以降に体細胞胚の形成が確認できます。この組織を単離して培養することで、根や茎葉の成長が進み、花を咲かせて種子を実らせました。胚組織は、その形態だけでなく、脂質と結合する試薬で染色することで他の器官と区別が容易になり、再生率や再生数などの定量化が可能です(図1)。
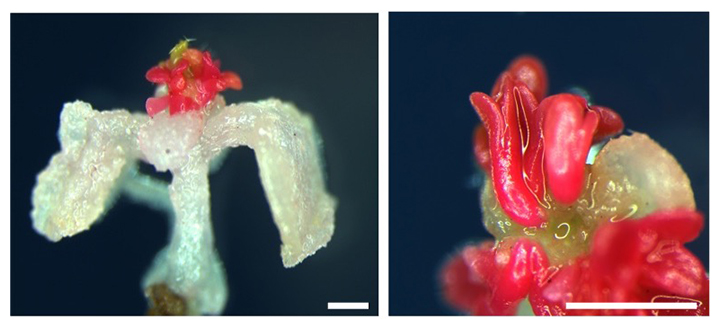
図1 WIND1の発現誘導による茎葉から胚への運命転換
WIND1を発現させたXVE-WIND1植物体の芽生えに誘導される体細胞胚(不定胚)。胚を特異的に染める試薬で染色した。赤い組織が体細胞胚。右は植物体の体細胞胚を拡大したもの。スケールバー:1mm。
共同研究グループのこれまでの研究や、国内外の研究から、植物の再生現象においてもエピジェネティックな制御が重要であることが分かってきています。そこで、このWIND1による体細胞胚誘導の実験系にさまざまなヒストン化学修飾阻害剤を添加する実験を行ったところ、ヒストン脱アセチル化阻害剤(Ky-2やRomidepsin)を加えた際や、ヒストンアセチル化阻害剤(MB-3)を加えた際に、体細胞胚の誘導が抑制されることを発見しました。この結果は、WIND1による体細胞胚誘導には、ヒストンの脱アセチル化とアセチル化の両方が必要であることを示します。
これらのヒストン化学修飾には、それぞれヒストン脱アセチル化酵素(HDAC)[8]とヒストンアセチル化酵素(HAT)[8]が必要です。WIND1はHDACやHATとどのように関係するのでしょうか。タンパク質同士の相互作用を検知できる種々の実験から、WIND1はHDACの一つであるHDA9という因子と直接結合すること、またそれぞれHATの一つであるHAG1やHAG3とは、ADA2という別のタンパク質を介して結合することが分かりました。実際、HDA9や、HAG1の機能を遺伝子発現レベルで抑えたXVE-WIND1植物体では、WIND1の発現を誘導しても体細胞胚がつくられませんでした(図2)。この結果は、WIND1による体細胞胚の誘導には、HDA9やHAG1が必要であることを示しています。
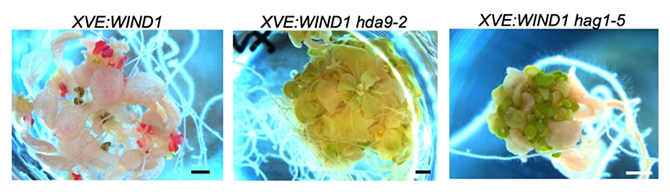
図2 WIND1による体細胞胚誘導に必要なHDA9やHAG1
XVE-WIND1植物体でHDA9やHAG1の機能を抑えると体細胞胚が誘導されなくなる。赤い組織が体細胞胚。スケールバー:1mm。左:体細胞胚を再生したXVE-WIND1植物体。中:XVE-WIND1でHDA9遺伝子を破壊した植物体。右:XVE-WIND1でHAG1遺伝子を破壊した植物体。いずれもWIND1遺伝子を発現させている。
また、WIND1タンパク質のどの部分にHDA9やADA2タンパク質が結合するかについて調べたところ、両者はWIND1タンパク質のN末端[9]領域に保存されているドメイン[10]に結合していることが分かりました。このドメインのアミノ酸配列を削ったWIND1(ΔN1WIND1)と、ドメインの中で保存されているアミノ酸の種類を変えたWIND1(mN1WIND1)は、HDA9やADA2が結合しなくなるだけでなく、発現を誘導しても体細胞胚をつくらなくなりました。この結果は、WIND1による体細胞胚の誘導には、WIND転写因子群によく保存されているこのドメインが必要であることを示しています。
では、WIND1の発現によって、実際ヒストンのアセチル化レベルに変化が出ているのでしょうか。これを網羅的に調べるために、XVE-WIND1植物体の茎葉を用いて、クロマチン免疫沈降-シークエンス(ChIP-seq)実験[11]を行いました。今回の研究では、ヒストンH3テールの27番目のリシンのアセチル化(H3K27Ac)[12]に特に注目しました。この結果、WIND1によって時間経過とともにアセチル化レベルが下がる遺伝子領域群と、逆にアセチル化レベルが上がる遺伝子領域群が明確に分かれることが示されました(図3)。この結果は、WIND1-HDAC複合体と、WIND1-ADA2-HAT複合体のターゲットとなるクロマチン(ヒストンタンパク質にDNAが巻き付いてできた複合体)領域が、何らかの作用によって正確に決められていることを示唆しています。
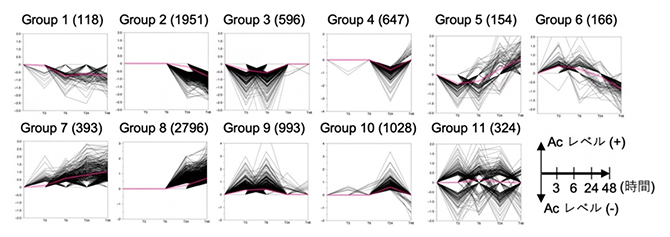
図3 WIND1の発現によるヒストンアセチル化レベルの変化
WIND1発現誘導後48時間目までにヒストンアセチル化(H3K27Ac)レベル(図ではAcレベル)が変わる遺伝子領域の変化パターンによるグループ分け。赤い線は0時間目でのアセチル化レベルを表す。ゲノム領域特異的にヒストンの脱アセチル化とアセチル化が起きていることが分かる。かっこの数字は領域の数。Acレベル(+)は上昇、Acレベル(-)は下降を表す。
ヒストンの脱アセチル化は、それを受けるクロマチン領域の遺伝子発現に対して抑制的に働きます。また逆に、ヒストンのアセチル化は遺伝子発現に対して促進的に働きます。WIND1の発現誘導後に発現量が変化する遺伝子の情報を、RNA-seq法(次世代シーケンサーを用いて遺伝子発現を網羅的に解析する手法)を用いて取得したところ、実際、WIND1-HDAC複合体のターゲットとなる遺伝子群と、WIND1の誘導で発現レベルが下がる遺伝子群は、統計的に有意に重なることがベン図解析[13]から明らかになりました。同様にWIND1-ADA2-HAT複合体のターゲットとなる遺伝子群とWIND1の発現誘導によって発現レベルが上がる遺伝子群も統計的に有意に重なりました。この結果は、WIND1による遺伝子発現制御には、ヒストンのアセチル化を介したエピジェネティックな制御も関与していることを示しています。
WIND1-HDAC複合体のターゲットとなり、発現が抑制する遺伝子群では、茎葉の分化状態を決める転写因子や、光合成に関与する遺伝子群、細胞分裂に関与する遺伝子群などが有意に見られました(図4左)。逆に、WIND1-ADA2-HAT複合体のターゲットとなり、発現が促進する遺伝子群には、予想通り胚発生に関与する転写因子群が見られた他、細胞のリプログラミング(初期化)に関与する重要な転写因子群や、道管形成に関与する転写因子群、また、防御応答に関与する遺伝子群などが統計的に有意に見られました(図4右)。
この結果から、WIND1はパートナーとなるヒストン修飾因子を変えることで、茎葉の分化状態の抑制と、新しい発生運命の獲得や防御応答を制御していることが分かりました。また、WIND1の発現誘導後に、ヒストン修飾阻害剤を短時間(1~3日間)処理する実験から、HDACとの複合体がHATとの複合体よりも先に作用していることが予想されました。つまり、WIND1はまず茎葉の分化状態の抑制を行い、その後新しい運命を獲得させていることが示唆されました。
共同研究グループはさらに、HDACとの複合体や、HATとの複合体のターゲットとなる重要因子について詳細に解析を進めました。この解析から、葉などの器官原基の発生を制御するANTという転写因子の遺伝子や、植物ホルモンであるサイトカイニンへの応答の負の制御因子として知られるSPL9という転写因子の遺伝子がHDACとの複合体のターゲットとして抽出されてきました(図4左)。実際、これらの遺伝子発現はWIND1誘導後に顕著に抑制されることが分かりました。ところが、XVE-WIND1植物体の培養系にHDAC阻害剤を添加したり、XVE-WIND1植物体でHDA9遺伝子の機能を抑えたり、またN末端領域に保存されているドメインを削ったりしたXVE-ΔN1WIND1植物体では、この遺伝子発現抑制は起きなくなりました。この結果は、WIND1によるこれらの遺伝子発現抑制がHDA9やWIND1のN末端配列に依存することを示しています。
HATとの複合体のターゲットとなる重要因子として、植物の胚発生や体細胞胚の誘導に関与するLEC2転写因子と、傷害応答性の細胞リプログラム因子であるERF115という転写因子について着目しました(図4右)。これらの遺伝子発現はWIND1誘導後に顕著に促進することが分かりました。予想通り、XVE-WIND1植物体の培養系にHAT阻害剤を添加したり、XVE-WIND1植物体でHAG1遺伝子の機能を抑えたり、またN末端領域に保存されているドメインを削ったXVE-ΔN1WIND1植物体では、この遺伝子発現の促進は起きなくなりました。この結果は、WIND1によるこれらの遺伝子発現の促進は、HAG1やWIND1のN末端配列に依存することを示しています。
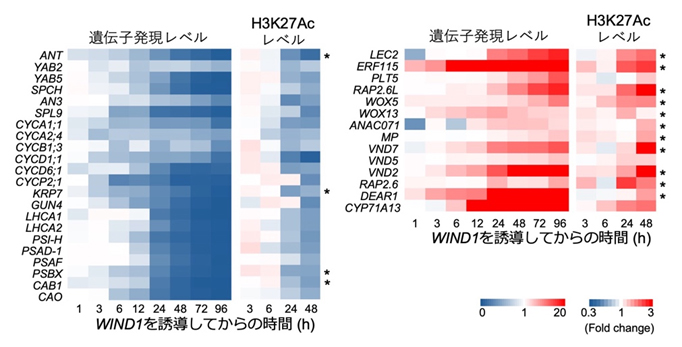
図4 WIND1誘導後に遺伝子発現およびH3K27Acレベルの変化を示す重要因子
(左)ヒストンアセチル化レベルが下がり、かつ遺伝子発現が抑制される遺伝子には茎葉の分化状態を規定する遺伝子や細胞分裂、光合成関連遺伝子が多かった。(右)ヒストンアセチル化レベルが上がり、かつ遺伝子発現も促進される遺伝子には、細胞リプログラミング因子、道管形成因子や防御応答に関わる転写因子が多く見られた。アスタリスク(*)は、その遺伝子の近傍にWIND1が結合することを示している。色は0時間時と比べて変化量が減ったもの(青)と増えたもの(赤)を表している。
この結果を受けて、WIND1による体細胞胚の誘導にLEC2やERF115の両転写因子が必要であるかについて検討したところ、XVE-WIND1植物体でLEC2遺伝子を働かなくさせた場合には、体細胞胚の誘導が全く起こらなくなったのに対し、ERF115遺伝子を働かなくさせても体細胞胚がERF115遺伝子を働かせたときと同じように誘導されました。これらの結果から、WIND1による体細胞胚の誘導には、LEC2遺伝子の機能が必須であることが分かりました。またERF115遺伝子は、この体細胞胚の誘導には関与しないことが明らかとなりました。
WIND1によるヒストン修飾の作用をより深く理解するために、WIND1転写因子がゲノム上のどこに結合するのかについて、ChIP-seq法を用いた網羅的解析を進めました。WIND1の結合部位とアセチル化(H3K27Ac)の変化が生じる領域との重なりを調べたところ、WIND1が直接結合する領域とヒストンアセチル化が抑制される領域は統計的に有意には交わらないのに対し、ヒストンアセチル化が促進される領域は有意に交わることが分かりました。実際、WIND1が結合し、H3K27Acレベルの低下と遺伝子発現の抑制が起こる遺伝子領域では、(A/C)CACAという配列がWIND1の結合し得る配列として有意に検出されてくるのに対し、逆のケース、すなわちH3K27Acレベルの上昇と遺伝子発現の促進が起こる遺伝子領域では、GCC box[14]として知られる(A/G)CCGNC配列が有意に検出されてきました。これらの結果から、WIND1によるヒストン脱アセチル化制御とアセチル化制御は、異なる分子機構によって成立していることが示唆されました。
今後の期待
植物の再生能力を理解し制御することは、農業や園芸、バイオテクノロジーなど植物を基盤とする産業において、今後ますます重要になると考えられます。多くの植物種では再生能力が低いため、ゲノム編集などによる機能改変や品種改良の研究が進みにくいという課題があります。本研究の成果を基に、植物の再生機構を分子レベルで解明し、その制御法を確立することができれば、これまで研究や育種が困難だった、野菜や果樹といった植物種にも応用が広がり、植物関連産業の発展や新たな経済的・社会的価値の創出につながると期待されます。また今後、WIND1がヒストン修飾タンパク質との相互作用をどのように切り替え、どのように狙った遺伝子の発現をオン/オフしているのかを明らかにすることで、新しい遺伝子発現の制御機構の理解や、その応用技術の開発につながる可能性があります。
補足説明
- 1.転写因子
特定のDNA配列に結合し、遺伝子発現を制御するタンパク質の一群。遺伝子発現のスイッチに例えられ、遺伝子発現を促進するものを転写活性化因子、抑えるものを転写抑制因子と呼ぶ。 - 2.発生運命
細胞が将来どのような細胞や組織になるかという「将来の役割」のこと。例えば植物では、受精卵が分裂と細胞分化を繰り返し葉や根、花など異なる組織を生み出すが、その進む先がどれになるのかという細胞の方向性を発生運命と呼ぶ。 - 3.カルス
植物の分野では傷害部位に形成する細胞塊(さいぼうかい)を示す言葉であり、癒傷組織(ゆしょうそしき)とも呼ばれる。現在では、広く組織培養条件下で組織片から生じる細胞塊を示す言葉として使われている。カルスが生じることをカルス化と呼ぶ。 - 4.道管
維管束植物が持っている水や光合成でつくった糖などの栄養を運ぶための通道組織のうち、水や無機養分を運ぶための管。栄養を運ぶための管は篩管(しかん)と呼ぶ。 - 5.体細胞胚(不定胚)
受精卵からではなく、体細胞から生じる胚。体細胞胚と不定胚は同義。通常の受精卵と同様な形態的変化の過程を取ることが知られている。組織培養条件下では、単離した一つの体細胞から不定胚を経由し、完全な植物体をつくることから、不定胚形成は分化全能性発揮の一つの指標となる。 - 6.ヒストンのアセチル化と脱アセチル化
DNAの働きを調節するエピジェネティック([7]参照)な仕組みの一つ。DNAはヒストンと呼ばれるタンパク質に巻き付いて細胞内に収納されているが、ヒストンにアセチル基という化学修飾が付く(アセチル化)とDNAが緩み、遺伝子が働きやすくなることが知られている。逆に、アセチル基が取り除かれる(脱アセチル化)とDNAが再び強く巻き付くため、遺伝子は働きにくくなる。このようなヒストンの化学修飾の変化によって、細胞は必要な遺伝子の働きを調節している。 - 7.エピジェネティック修飾、エピジェネティック
DNAの配列そのものを変えずに、遺伝子の働き方を調節する仕組みのことをエピジェネティックな制御という。DNAやそれを巻き取っているヒストンタンパク質に化学的な修飾(エピジェネティック修飾)が加わることで、特定の遺伝子が働きやすくなったり、逆に働きにくくなったりする。 - 8.ヒストン脱アセチル化酵素(HDAC)、ヒストンアセチル化酵素(HAT)
どちらもヒストンに付くアセチル基という化学修飾を調節する酵素。HATはヒストンにアセチル基を付加することでDNAの巻き付き方を緩め、遺伝子が働きやすい状態をつくる。一方、HDACはヒストンからアセチル基を取り除き、DNAを再び強く巻き付かせることで遺伝子の働きを抑える方向に作用する。このように両者は拮抗的に働きながら、細胞内での遺伝子発現を細かく調節している。 - 9.N末端
タンパク質はアミノ酸同士が脱水縮合して形成されたポリマーであり、隣接するアミノ酸は、それぞれのアミノ基とカルボキシ基がペプチド結合をしている。このポリマーの末端のフリーのアミノ基側をN末端、カルボキシ基側をC末端と呼ぶ。 - 10.ドメイン
タンパク質の中で特定の働きを担う構造的・機能的なまとまりの部分のこと。多くのタンパク質は複数のドメインから構成されており、それぞれが他のタンパク質やDNAと結合するなど、異なる役割を担っている。このようにドメインの組み合わせによって、タンパク質はさまざまな機能を発揮することができる。 - 11.クロマチン免疫沈降-シークエンス(ChIP-seq)実験
特定のタンパク質がゲノムDNAのどの領域に結合しているかを網羅的に調べる実験手法。まず、DNAとそれに結合しているタンパク質の複合体(クロマチン)を細胞から取り出し、目的のタンパク質に特異的に結合する抗体を用いてその複合体を回収する。その後、回収されたDNA断片の配列を次世代シークエンサーで解析することで、そのタンパク質がゲノム上のどの場所に結合しているかを明らかにすることができる。 - 12.ヒストンH3テールの27番目のリシンのアセチル化(H3K27Ac)
ヒストンH3というタンパク質の27番目のリシン(K)残基にアセチル基(Ac)が付加された状態を示すヒストン(エピジェネティック)修飾の一種である。この修飾は、遺伝子の発現が活発に行われている領域や、遺伝子の働きを調節するエンハンサー領域などに多く見られることが知られている。そのため、H3K27Acはゲノム上で活性化している遺伝子調節領域を示す指標として、遺伝子発現制御の研究で広く用いられている。 - 13.ベン図解析
複数のデータ集合の共通部分や違いを視覚的に示すための解析方法。円などの図形を重ねて表現することで、それぞれのデータに特有の要素と、複数のデータに共通して含まれる要素を直感的に示すことができる。遺伝子研究では、異なる実験条件で得られた遺伝子リストなどを比較し、共通して変化する遺伝子や条件特異的な遺伝子を見つけるためによく用いられる。 - 14.GCC box
植物のDNA上にある特定の短い配列。遺伝子の働きを調節する目印のような役割を持つ。AP2/ERF転写因子群(WIND1も含まれる)が結合することで、傷害応答やストレス応答などに関わる遺伝子の発現を調節する。一般に、植物が環境の変化に応じて遺伝子の働きを切り替えるための重要な制御配列の一つ。
共同研究グループ
理化学研究所 環境資源科学研究センター
細胞機能研究チーム
上級研究員 岩瀬 哲(イワセ・アキラ)
(科学技術振興機構(JST)さきがけ研究員)
テクニカルスタッフⅡ 竹林 有理佳(タケバヤシ・アリカ)
研究員(研究当時)フン・フユ(Fu-YU Hung)
(現 台湾国立中興大学 農業自然資源学院 助教授、現 細胞機能研究チーム 客員研究員)
テクニカルスタッフⅠ 河村 彩子(カワムラ・アヤコ)
基礎科学特別研究員 インジェ・エトキン・チャカ(Yetkin çaka Ince)
チームディレクター 杉本 慶子(スギモト・ケイコ)
(東京大学 大学院理学系研究科 教授)
植物免疫研究グループ
専任研究員 門田 康弘(カドタ・ヤスヒロ)
グループディレクター 白須 賢(シラス・ケン)
(東京大学 大学院理学系研究科 教授)
東京大学 大学院理学系研究科
准教授 稲垣 宗一(イナガキ・ソウイチ)
中部大学 応用生物学部
教授 鈴木 孝征(スズキ・タカマサ)
研究支援
本研究は、科学技術振興機構(JST)戦略的創造研究推進事業さきがけ「植物分子の機能と制御」研究領域の「低分子化合物から読み解く植物細胞の分化全能性(研究代表者:岩瀬哲、JPMJPR20D2)」、同先端国際共同研究推進事業「TOPチームのためのASPIRE」の「植物の誘導リプログラミングに立脚した新規バイオエコノミー基盤の創出(研究代表者:杉本慶子、JPMJAP2306)」、同革新的GX技術創出事業「バイオものづくり」研究領域の「先端的植物バイオものづくり基盤の構築(研究代表者:大熊盛也、主たる共同研究者:杉本慶子、JPMJGX23B0)」「GXを駆動する微生物・植物『相互作用育種』の基盤構築(研究代表者:野村暢彦、主たる共同研究者:白須賢、JPMJGX23B2)」、日本学術振興会(JSPS)科学研究費助成事業基盤研究(C)「体細胞胚誘導の分子メカニズム(研究代表者:岩瀬哲、JP20K06694)」「分化全能性発揮の運命転換を制御するWIND1-ヒストン修飾因子複合体の機能解析(研究代表者:岩瀬哲、JP24K09494)」、同学術変革領域研究(B)「プラスチド相転換を制御する因子の機能解析(研究代表者:岩瀬哲、JP22H05075)」、同学術変革領域研究(A)「植物の環境レジリエンスを支える傷害修復機構(研究代表者:杉本慶子、JP20H05911)」、同特別研究員奨励費「植物メリステムで細胞増殖をエピジェネティックに制御する仕組みの解明(研究代表者:杉本慶子、JP23KF0089)」、同基盤研究(B)「植物の器官再生を支える細胞リプログラミング制御機構の解明(研究代表者:杉本慶子、JP24K02051)」による助成を受けて行われました。
原論文情報
- Akira Iwase, Arika Takebayashi, Fu-Yu Hung, Ayako Kawamura, Yetkin çaka Ince, Yasuhiro Kadota, Soichi Inagaki, Takamasa Suzuki, Ken Shirasu, Keiko Sugimoto, "WIND1 controls cell fate transition through coordinately integrating histone acetylation and deacetylation-mediated transcriptional reprogramming during somatic embryogenesis", Molecular Plant, 10.1016/j.molp.2026.03.005
発表者
理化学研究所
環境資源科学研究センター 細胞機能研究チーム
上級研究員 岩瀬 哲(イワセ・アキラ)
チームディレクター 杉本 慶子(スギモト・ケイコ)
 左から岩瀬哲、杉本慶子
左から岩瀬哲、杉本慶子
報道担当
理化学研究所 広報部 報道担当
お問い合わせフォーム
