理化学研究所(理研)バイオリソース研究センター 実験動物開発室の仲柴 俊昭 専任研究員、吉木 淳 室長、疾患ゲノム動態解析技術開発チーム(研究当時)の阿部 訓也 チームリーダー(研究当時、現 iPS細胞高次特性解析研究チーム 客員主管研究員)、脳神経科学研究センター 細胞機能探索技術研究チームの宮脇 敦史 チームディレクターらの共同研究グループは、マウス遺伝子操作において見過ごされてきた問題点である「遺伝子発現の抑制漏れ」について、高感度発光技術・AkaBLI[1]を利用して正確に評価し、さらに「漏れ」を抑える手法を検討し、遺伝子操作の精度を飛躍的に向上させることに成功しました。
本研究成果は、今後、がんや脳機能の研究など、極めて精密な操作が求められる医学・生命科学研究において、より信頼性の高いデータの取得を可能にすると期待されます。
今回、共同研究グループは、マウスの特定の細胞や組織において行うCre-loxPシステム[2]による遺伝子操作を、体外から評価できるレポーターマウス[3]を開発するため、複数の遺伝子改変マウスを作製しました。その結果、遺伝子発現を転写レベルで制御する従来の手法では、遺伝子を発現しないよう制御した状態でも微量な発現が起こってしまう「遺伝子発現の抑制漏れ」があることを突き止めました。この「漏れ」は遺伝子操作の精度を損なう要因となります。一方、遺伝子発現を転写と翻訳の2段階で制御する新たな手法では「漏れ」を最小限に抑えることができ、Cre-loxPシステムによる遺伝子操作を体外から正確に評価できるレポーターマウスの開発に成功しました。
本研究は、科学雑誌『Cell Reports Methods』オンライン版(3月30日付:日本時間3月31日)に掲載されました。
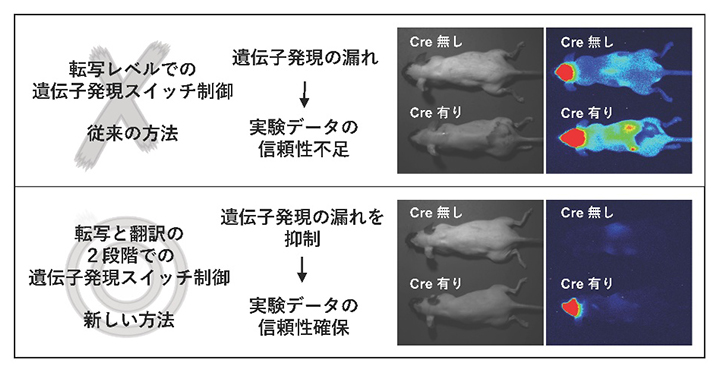
「遺伝子発現の抑制漏れ」を最小限に抑えた遺伝子改変の新手法
背景
生体内の特定の部位や時期に限定して遺伝子機能を発現させる「遺伝子発現スイッチ」は、現代の生命科学研究において不可欠な基盤技術であり、Cre-loxPシステムが定番のツールとして使われます。しかし、このシステムには、スイッチが「オフ」の状態でも遺伝子が微量に発現してしまう「遺伝子発現の抑制漏れ(リーク)」という長年の課題がありました。この「漏れ」は実験データの信頼性を損なう要因となりますが、その程度を定量的に評価する手法は確立されていませんでした。
共同研究グループは先行研究で、「高感度発光技術・AkaBLI」を導入した生体内(in vivo)発光イメージング[4]によって、この「遺伝子発現の抑制漏れ」が可視化・定量化可能であることを見いだしました注1)。今回の研究では、この評価系を活用し、「遺伝子発現の抑制漏れ」を高度に抑制する新たな手法の開発とその有効性の検証に取り組みました。
- 注1)2023年9月8日プレスリリース「生体深部を非侵襲的に観察できる多色発光イメージング用マウス」
研究手法と成果
Cre-loxPシステムは、細胞種選択的に遺伝子発現を操作する遺伝子工学技術の一つです。DNA組換え酵素「Cre」が「loxP配列」と呼ばれる特定の遺伝子配列を認識し、部位特異的な組換えを引き起こします。
このCre-loxPシステムを使った従来の手法では、Creが発現する細胞・組織・臓器で遺伝子発現をオンにできるよう、mRNAの転写を制御する配列(STOP配列[5])を組み込んだ遺伝子発現カセット(小断片)が広く利用されてきました。共同研究グループは、世界最高感度の発光技術「AkaBLI」に用いられる発光酵素「Akaluc」注2)を発現させる遺伝子発現カセットをデザインし、これを用いてレポーターマウスを作製しました。
その結果、Creが作用する前の段階で「遺伝子発現の抑制漏れ」が生じていることをAkaBLIによって検出し、この「漏れ」が実験データの正確な解釈を困難にしていることを示しました(図1A、図2上段)。
そこで、Akaluc発光レポーター遺伝子の発現をmRNAの転写とタンパク質の翻訳の2段階で制御できるよう、遺伝子発現カセットに改良を加えたところ、Creが作用する前段階での「遺伝子発現の抑制漏れ」を最小限に抑えることができました(図1B、C、図2A下段)。
この新技術を導入したレポーターマウスを用いることで、標的部位で遺伝子発現が正確に変化したかどうかを、生体外から鮮明な「光」として捉えることが可能になりました。例えば、体表面から離れた脳深部に位置する神経伝達物質ドーパミンを放出する神経細胞[6]の存在も、体外から正確に検出できます(図1D、図2B下段)。
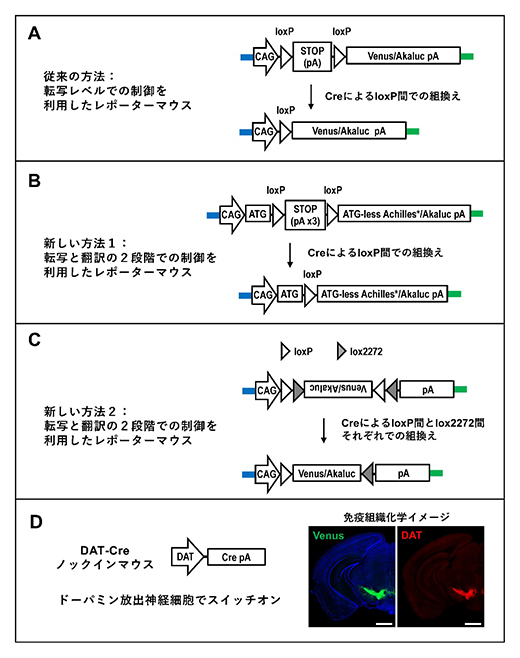
図1 遺伝子発現スイッチの仕組み
- (A)mRNAの転写を制御するSTOP配列(転写を止めるpolyA(pA)配列)を組み込んだ遺伝子発現スイッチ(従来の方法)。DNA組換え酵素「Cre」が働くと、loxPのペア間で組換えが生じてSTOP配列が取り除かれる。その結果、とても強い遺伝子発現活性を持つCAGプロモーターが蛍光(Venus)と発光(Akaluc)タンパク質の遺伝子発現を指示する。
- (B)転写・翻訳の2段階制御(新しい方法1):STOP配列による転写制御に加え、翻訳開始シグナル(ATG)を分離。Creの働きで配列がつながり、蛍光(Achilles)とAkalucの両タンパク質が正しく発現する。
- (C)転写・翻訳の2段階制御(新しい方法2):遺伝子を逆向きに配置して転写を阻止。Creによる組換え(loxP/lox2272)で向きを正し、両タンパク質の発現を誘導する。
- (D)ドーパミン放出神経細胞でCreを発現するDAT-Creノックインマウスにより、遺伝子発現のスイッチオン。DATはドーパミントランスポーターの略であり、ドーパミン放出神経細胞でDATタンパクが発現している(赤色)。VenusとAkalucのタンパク質(緑色)は、頭頂部表面から離れた脳深部の細胞で発現している。白スケールバーは1mm。
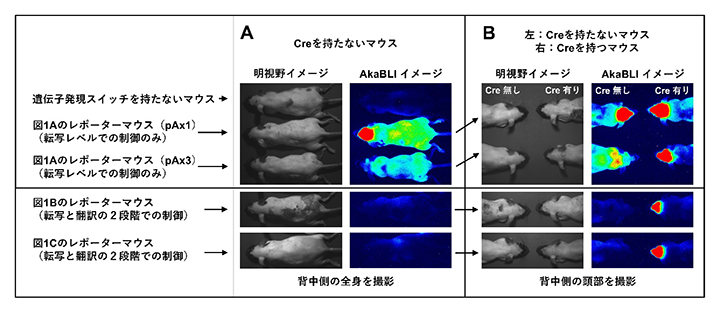
図2 AkaBLIによる遺伝子発現スイッチの検証
- (A)「漏れ」の検証:転写レベルのみの制御では「遺伝子発現の抑制漏れ」によるAkaBLIシグナルが検出されたが(上段)、転写・翻訳の2段階で制御するとシグナルは消失した(下段)。これにより、スイッチの「漏れ」が最小限に抑えられていることが確認された。転写レベルでの制御のみを持つレポーターマウスは2種類(pAを一つ、またはpAを三つ持つ)で検証。
- (B)「有効性」の検証:転写レベルでの制御のみでは、「漏れ」によるノイズのため脳深部の標的細胞(Cre有り)との差が不明瞭になり、解析を困難にしている(上段)。制御を二重化したレポーターマウスではCreを持たない個体での「漏れ」が抑えられているため、DAT-Creを持つ個体の頭部で検出されたシグナルが、ドーパミン放出神経細胞由来であることを正確に特定できる(下段)。
また、Akaluc発光レポーターでの標識に用いたCreマウスにおいて、ドーパミン放出神経細胞だけでなく、体内の他の部位でも遺伝子操作が誘発されていることが判明しました(図3)。こうした精密な解析は、遺伝子発現の「漏れ」を極限まで抑制したことで、初めて実現したものです。
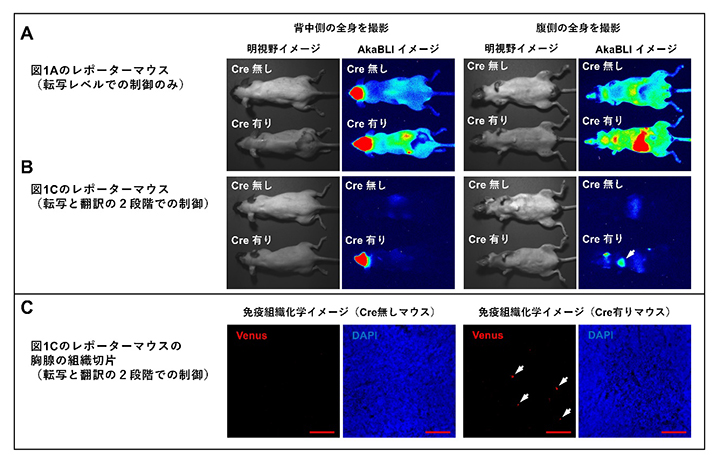
図3 高精度レポーターマウスによる全身の遺伝子操作部位の評価
- (A)転写制御のみの課題:Creの有無によるAkaBLIシグナル差が不明瞭で、遺伝子操作部位の特定が困難。
- (B)二重制御の有効性:転写・翻訳の2段階で制御するとシグナル差が明確になり、頭部(ドーパミン放出神経細胞、中央パネル)以外に胸部での発現(右パネル、矢印)も新たに発見。
- (C)組織レベルでの確認:胸部(胸腺)の組織切片において、実際に遺伝子操作されたVenus陽性細胞を確認(右パネル、矢印)。赤スケールバーは100マイクロメートル(μm、1μmは100万分の1メートル)。
特定の細胞・組織・臓器において遺伝子操作を行うために、これまでに多数の「Creマウス」が開発されてきました。しかし、これらCreマウスによる遺伝子操作の特異性を、全身で包括的に評価できるレポーターマウスはこれまで存在しませんでした。
今回開発した新型レポーターマウスを用いることで、多様なCreマウスが誘発する全身各部位の遺伝子操作を、AkaBLI技術によって体外から非侵襲的に評価することが可能となりました(図4)。
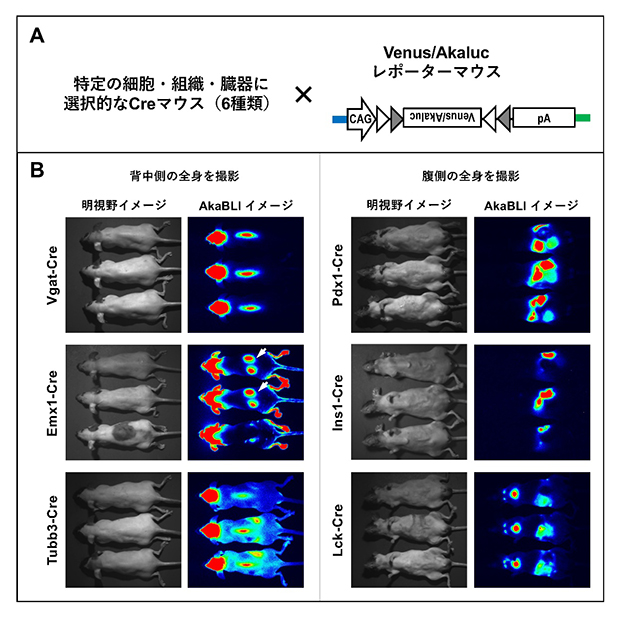
図4 代表的なCreマウスライブラリーの全身での遺伝子操作部位の評価
- (A)評価方法:6種類の代表的なCreマウスを、「漏れ」を抑えた高精度レポーターマウスと交配させて、各Cre酵素が実際に働く部位を正確に評価。
- (B)6種類のCreマウスが誘発する全身各部位の遺伝子操作を、AkaBLI技術によって体外から非侵襲的に評価した。背中側(左)と腹側(右)の全身。
Vgat-Cre:頭部・背骨(抑制性神経)。Emx1-Cre:頭部(大脳皮質)に加え、腎臓(矢印)、四肢。Tubb3-Cre:頭部・背骨に加え、全身の感覚神経など。Pdx1-Cre:腹部(膵臓、十二指腸)。Ins1-Cre:腹部(膵臓のインスリン産生細胞)。Lck-Cre:胸腺、リンパ節(T細胞)。
- 注2)2018年2月23日プレスリリース「脳の深部を非侵襲的に観察できる人工生物発光システムAkaBLI」
今後の期待
今回、AkaBLIを用いた定量的な評価系によって「遺伝子発現の抑制漏れ」を克服したことは、遺伝子工学における長年の課題に対する一つの解となるものです。
この高精度なレポーターマウスは、既存の多様なCreマウスライブラリー[7]の再評価を可能にするだけでなく、より厳密な時間空間制御が必要な疾患モデルマウスの作製においても標準的な手法となることが期待されます。本成果が、複雑な生物学的プロセスを個体レベルでより正確に理解するための強力なツールとなり、生命科学研究のさらなる発展に寄与することを確信しています。また、「遺伝子発現の抑制漏れ」を抑える技術を応用することで、これまで解析が困難であった微細な生命現象の解明が進み、創薬研究や次世代の治療法開発を加速させる重要な基盤となることが展望されます。
補足説明
- 1.高感度発光技術・AkaBLI
ホタルは「ルシフェリン(光る物質)」と「ルシフェラーゼ(光らせる酵素)」の反応で光る。AkaBLIは、この仕組みを人工的に改良し、従来の100~1,000倍という圧倒的な明るさを実現した高感度発光技術である。ルシフェリンとしてAkaLumineという光る物質、ルシフェラーゼとしてAkalucという光らせる酵素を使用。AkaBLIはAka bioluminescent imagingの略。 - 2.Cre-loxPシステム
狙った場所やタイミングで遺伝子を自由に操作するための、バイオテクノロジーの定番ツール。Cre酵素はDNA上の目印となるloxPを認識してつなぎ変える。これにより、生体内の特定の場所だけで遺伝子の発現スイッチを「オン・オフ」にできる。 - 3.レポーターマウス
レポーターマウスは、体内で特定の遺伝子が働く場所や時間を、光(蛍光や発光)によって観察できるように改良された実験用マウス。通常、いつ・どの細胞で遺伝子が活動しているかを見ることはできないが、レポーター遺伝子を組み込むことによってその遺伝子の活動を知ることができ、このマウスを用いることで、生命現象をリアルタイムで「見える化」できる。今回のレポーターマウスは、Akaluc遺伝子の発現によりAkalucレポータータンパクの発光現象を通して遺伝子操作の部位を観察できるようにしたもの。 - 4.生体内(in vivo)発光イメージング
生体内で発光する細胞からのシグナルを体外からイメージングする。AkaBLIでは、Akaluc遺伝子を発現させることで細胞を標識し、AkaLumineを動物へ投与して発光させる。動物を傷つけることなく、生きたままの脳の深い場所や、たった1個のがん細胞の動きまで、体外から観察することができる。 - 5.STOP配列
遺伝子が読み取られるのを途中で強制的にストップさせる、特殊なDNAのブレーキ役。遺伝子の転写をSTOPさせるpolyA(pA)配列がよく使われる。この配列の両端に「loxP」を配置させると、Cre酵素によってSTOP配列が切り取られ、その先の遺伝子が転写されるようになり、Cre発現細胞で遺伝子の発現スイッチをオンにできる。 - 6.神経伝達物質ドーパミンを放出する神経細胞
脳の中で「ドーパミン」という情報を伝える物質をつくり、放出する神経細胞。マウスの頭頂部から4~5mmの深さのところにある。脳の「やる気」と「快楽」をコントロールする司令塔。この細胞が減ると「パーキンソン病」の原因になり、過剰に働くと依存症などに関わることが知られている。 - 7.Creマウスライブラリー
世界中で開発された、特定の細胞・組織・臓器で遺伝子を操作できる特別なマウス(Creマウス)の膨大なコレクション。数百種類のCreマウスがいる。複雑な体の仕組みをピンポイントで解明できるようになる。
共同研究グループ
理化学研究所
バイオリソース研究センター
実験動物開発室
専任研究員 仲柴 俊昭(ナカシバ・トシアキ)
テクニカルスタッフⅡ 岩間 瑞穂(イワマ・ミズホ)
室長 吉木 淳(ヨシキ・アツシ)
疾患ゲノム動態解析技術開発チーム(研究当時)
チームリーダー(研究当時)阿部 訓也(アベ・クニヤ)
(現 iPS細胞高次特性解析研究チーム 客員主管研究員)
脳神経科学研究センター 細胞機能探索技術研究チーム
チームディレクター 宮脇 敦史(ミヤワキ・アツシ)
客員研究員 岩野 智(イワノ・サトシ)
株式会社エビデント
シニアプロフェッショナル 杉山 崇(スギヤマ・タカシ)
研究支援
本研究は、日本学術振興会(JSPS)科学研究費助成事業研究活動スタート支援「大脳皮質の広領域動態解析の開発と応用(研究代表者:仲柴俊昭、JP26890026)」、同学術変革領域研究(B)「動的な生体酸素シグナルを解明する分子イメージング・オミクス技術の開発(研究代表者:口丸高弘、研究分担者:仲柴俊昭、JP25H01436)」、科学技術振興機構(JST)共創の場形成支援プログラムCOI-NEXT「つくば型デジタルバイオエコノミー社会形成の国際拠点」の助成を受けて行われました。
原論文情報
- Toshiaki Nakashiba, Takashi Sugiyama, Satoshi Iwano, Mizuho Iwama, Atsushi Yoshiki, Atsushi Miyawaki, Kuniya Abe, "Assessing leaky expression of Cre-dependent DNA constructs in the mouse genome using sensitive bioluminescent reporters", Cell Reports Methods, 10.1016/j.crmeth.2026.101369
発表者
理化学研究所
バイオリソース研究センター 実験動物開発室
専任研究員 仲柴 俊昭(ナカシバ・トシアキ)
室長 吉木 淳(ヨシキ・アツシ)
疾患ゲノム動態解析技術開発チーム(研究当時)
チームリーダー(研究当時)阿部 訓也(アベ・クニヤ)
(現 iPS細胞高次特性解析研究チーム 客員主管研究員)
脳神経科学研究センター 細胞機能探索技術研究チーム
チームディレクター 宮脇 敦史(ミヤワキ・アツシ)
報道担当
理化学研究所 広報部 報道担当
お問い合わせフォーム
