理化学研究所(理研)生命医科学研究センター 疾患エピゲノム遺伝研究チームの井上 梓 チームディレクターらの研究チームは、卵母細胞(卵)から受精後の胚(次世代)へと世代を超えて受け継がれるエピジェネティック修飾(エピゲノム)[1]の確立機構を解明しました。
本研究成果は、将来的に卵の形成不全や不育症の原因解明など、生殖医療分野への応用につながることが期待されます。
DNAを収納するヒストンタンパク質[2]には、さまざまな化学修飾(ヒストン修飾[2])が付与されます。これまで研究チームは、世代を超えて受け継がれる経世代エピゲノム[3]の一つとして、ヒストン修飾H3K27me3[3]を同定していました。卵形成過程で確立されたH3K27me3は次世代に伝承され、個体発生や胎盤形成に重要な役割を果たします。
今回、研究チームは、卵においてH3K27me3が確立される遺伝子の大多数には、抑制(オフ)マークであるH2Aub[4]と活性化(オン)マークであるH3K4me3[5]という、2種類の拮抗(きっこう)するヒストン修飾が付与されていることを見いだしました。正常な卵形成ではこのオン・オフのバランスである"遺伝子てんびん"がH2Aub優勢に保たれる(「オフ」側に傾く)ことでH3K27me3が確立される一方で、これがH3K4me3優勢となる(「オン」側に傾く)とH3K27me3が消失し、次世代の胎盤形成異常が引き起こされることを示しました。
本研究は、科学雑誌『Molecular Cell』オンライン版(4月13日付:日本時間4月14日)に掲載されました。

経世代エピゲノム(H3K27me3)を確立させる遺伝子てんびん
背景
生物の設計図であるゲノムは、細胞分裂のたびに母細胞から娘細胞へと受け継がれます。ただし、遺伝情報そのもの(DNA配列)だけでなく、「どの遺伝子をどのように使うか」という"細胞の記憶"も一緒に引き継がれます。この記憶を担う仕組みがエピゲノムです。
通常、世代が親から子へと切り替わる受精の瞬間に、卵や精子のエピゲノムの大部分はリセットされます。しかし一部のエピゲノムはリセットされず胚に受け継がれることがあり、これは「エピゲノムの経世代伝承」と呼ばれます。この現象は、遺伝学の枠組みを拡張し再定義するものであり、その仕組みの解明は、生命継承の原理の深い理解につながります。
井上 チームディレクターらは、哺乳類において、H3K27me3が次世代に受け継がれるエピゲノム記憶として機能することを明らかにしてきました注1)。H3K27me3は、卵巣内で卵が成長する過程で確立され、受精後の初期発生を通じて維持されて、母性ゲノムの遺伝子発現を抑制し(ゲノム刷り込み[6])、胚発生や胎盤形成に重要な役割を果たします。
一方で、卵形成過程でH3K27me3が正しく確立されないと、胎児の発育や胎盤形成に異常が生じます注2)。従って、「どのようにして卵がこの重要な記憶(H3K27me3)を確立するのか」を明らかにすることは、発生学や遺伝学の重要な課題です。
井上 チームディレクターらはこれまでに、遺伝子発現を抑えるヒストンH2Aのモノユビキチン[4]化修飾(H2Aub)がH3K27me3の確立に必要であることを報告していました注3)。しかし、H2AubがどのようにH3K27me3の確立を促すのか、その具体的な仕組みは明らかではありませんでした。
- 注1)Inoue, A. Noncanonical imprinting: intergenerational epigenetic inheritance mediated by Polycomb complexes. Current Opinion in Genetics & Development. DOI: 10.1016/j.gde.2022.102015
- 注2)2022年4月28日プレスリリース「母親ゲノムの記憶が胎児を育む」
Matoba, S. et al. Noncanonical imprinting sustains embryonic development and restrains placental overgrowth. Genes Dev. DOI: 10.1101/gad.349390.122 - 注3)2021年4月6日プレスリリース「卵の記憶は胎盤へ」
- 注4)Mei, H. et al. H2AK119ub1 guides maternal inheritance and zygotic deposition of H3K27me3 in mouse embryos. Nat. Genet. 53, 539-550 (2021). DOI: 10.1038/s41588-021-00820-3
研究手法と成果
研究チームは、H3K27me3の確立機構を調べるため、卵成長過程においてH2Aub、H3K27me3、その他のヒストン修飾がどのように変化するかを、微量クロマチン免疫沈降シーケンス法[7]を用いて詳しく観察しました。
具体的には、卵成長の完了までにH3K27me3が確立される遺伝子に着目して、初期段階からのエピゲノム状態をさかのぼって調べました(図1A)。その結果、初期段階ではまだ多くの遺伝子でH3K27me3は確立されておらず、その代わりに、H2Aub(遺伝子抑制(オフ)マーク)および遺伝子活性化(オン)マークとして知られるH3K4me3が存在していました(図1B)。すなわち、これらの遺伝子は「発現しそうな状態」にありながらも、H2Aubで抑制されていることが考えられました。一方で、H3K27me3は後期に蓄積していました(図1B)。これらの結果と、「発現している遺伝子に対してはH3K27me3が確立されにくい」という知見を合わせて、「卵ではH3K27me3の確立に向けて、オンマークを持つ遺伝子の発現がH2Aubによって初期段階から抑制され続けている必要がある」のではないかと考えました。

図1 経世代エピゲノム(H3K27me3)の確立に至る段階的な変化
- (A)初期、後期、成長卵の成長過程の卵巣の模式図。
- (B)各成長段階の卵におけるH2Aub、H3K27me3、H3K4me3の挙動の模式図。
この仮説を確かめるため、研究チームは卵成長の初期段階からH2Aubを欠損させた卵[8]を作製し、H3K27me3の分布と遺伝子発現を解析しました。その結果、H2Aubが失われると、H3K4me3を持つ遺伝子が実際に活性化し、同時にH3K27me3が消失することが分かりました(図2)。この結果は、「H2Aubがオンマークの付いた遺伝子の発現を抑え込むことで、H3K27me3の確立を促す」という仮説を支持しています。一方で、H3K4me3を持たない遺伝子は、H2Aubがなくても活性化せず、H3K27me3は正常に形成されていました。すなわち、もともとオンマークが存在していない不活性遺伝子は、積極的な抑制機構(H2Aub)がなくても、定常状態として「オフ」が保たれ、その結果としてH3K27me3が確立されたことが考えられます。
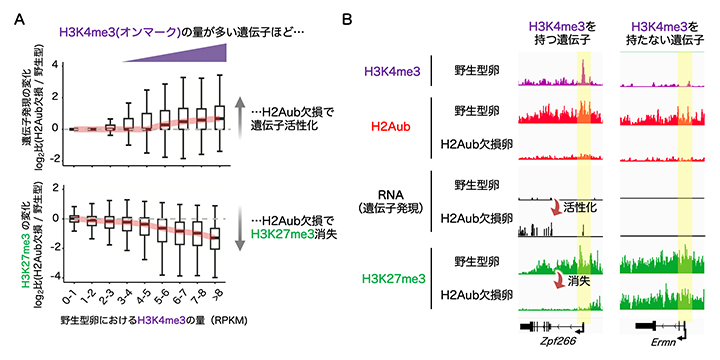
図2 H2Aub欠損卵の遺伝子発現およびエピゲノム解析
- (A)H2Aub欠損卵における遺伝子発現量(上図)とH3K27me3(下図)の変化。H3K27me3保有遺伝子を、転写開始点近傍領域におけるH3K4me3の量に応じて8グループに分類した(X軸、RPKMはReads Per Kilobase per Million mapped readsを示す)。H3K4me3が豊富な遺伝子ほど、H2Aub欠損下において遺伝子発現が上昇し、H3K27me3が消失することが分かる。
- (B)H3K4me3を持つ遺伝子と持たない遺伝子の例。転写開始点近傍領域(黄色ハイライト)にH3K4me3を持つ遺伝子では、H2Aub欠損下において遺伝子発現の上昇とH3K27me3の消失が起こることが分かる。一方で、H3K4me3を持たない遺伝子では、H2Aub欠損下でも遺伝子発現は活性化せず、H3K27me3は確立される。
次に研究チームは、オフマーク(H2Aub)がない状態でオンマーク(H3K4me3)も同時になくした"二重欠損卵[9]"を作製し、オフ状態を人為的に再現しました。その結果、この二重欠損卵では、H3K4me3が消失した遺伝子において、オフ状態が再現され、H3K27me3が再確立されることが分かりました(図3A、B、C)。さらに、これらの卵を受精させて次世代の胚発生を観察したところ、H2Aub欠損卵由来の胚では刷り込み発現が乱れ、胎盤異常(過形成)が認められたのに対し、二重欠損卵由来の胚では刷り込み発現が回復し、正常な胎盤が形成されました(図3D)。
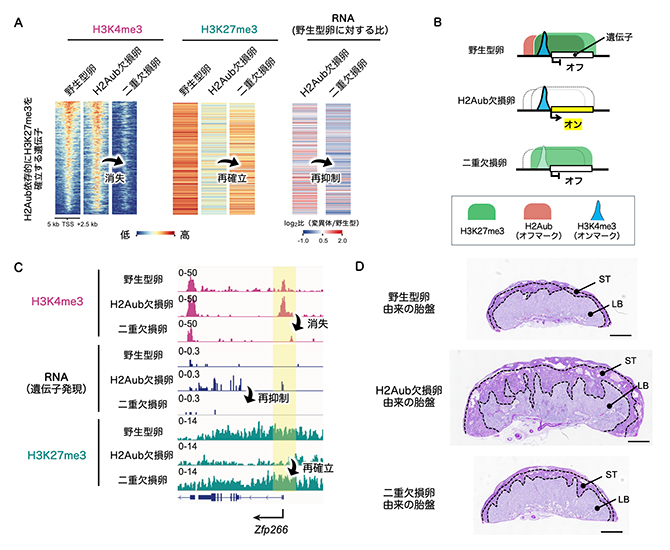
図3 H2Aub・H3K4me3二重欠損卵のエピゲノム解析と次世代の胎盤
- (A)H2Aub欠損卵およびH2Aub・H3K4me3二重欠損卵におけるエピゲノムと遺伝子発現変化のヒートマップ図。二重欠損卵ではH3K4me3が消失し、遺伝子発現の再抑制とH3K27me3の再確立が起こることが分かる。
- (B)結果の模式図。
- (C)H3K27me3が再確立される遺伝子の一例。転写開始点近傍領域(黄色ハイライト)のH3K4me3の消失により遺伝子発現が抑制され、H3K27me3が再確立することが分かる。
- (D)次世代個体の出生直前時点での胎盤の組織学的解析。H2Aub欠損卵由来の胎盤は、海面栄養芽層(ST)の増大と迷路層(LB)への浸潤に特徴付けられる過形成が認められる。二重欠損卵由来の胎盤は正常。スケールバーは1mm。
これらの成果から、卵形成過程では、遺伝子のオン・オフの拮抗バランスが存在し、そのバランスが「オフ」側に保たれることが、H3K27me3の確立と次世代の正常な胎盤形成に不可欠であることが示唆されました(図4)。

図4 本研究結果の概要図
経世代エピゲノム(H3K27me3)は、オフ(H2Aub)とオン(H3K4me3)の拮抗バランスの下流で確立される。野生型卵では、H2Aubが遺伝子をオフ状態に保つことでH3K27me3が正常に形成される(左)。H2Aub欠損卵ではオンマークが優勢となり、遺伝子をオフ状態に保つことができずH3K27me3は確立されない(中央)。H2Aub・H3K4me3二重欠損卵では、定常状態として遺伝子が発現せず(オフ状態)、H3K27me3が再確立される(右)。
今後の期待
本研究では、遺伝子のオン・オフのバランスが経世代エピゲノムの確立に欠かせないことを明らかにしました。このバランスが崩れると、次世代の胎盤形成にまで影響が及ぶことが分かりました。本研究により、卵が次世代へ伝えるべき情報をどのように準備するか、という世代継承の基本原理の一端が明らかになり、生殖医療や発生異常の理解にも新たな手掛かりを与えると期待されます。
今回の研究は、遺伝的介入により人為的に卵のエピゲノムバランスを崩して、その経世代的な影響を探求するものでした。今後、親世代の環境要因などによって卵のエピゲノムバランスが乱れ、次世代の発生に影響が及ぶことがあるか、といった経世代的な視点での研究展開につながることが期待されます。
補足説明
- 1.エピジェネティック修飾(エピゲノム)
細胞には、自身の膨大なゲノム情報から必要な情報だけを取り出すための「ゲノムの取扱説明書」のような機構が備わっている。エピジェネティック修飾はその主要な機構の一つである。 - 2.ヒストンタンパク質、ヒストン修飾
ヒストンタンパク質には、H2A、H2B、H3、H4の4種類がある。それらが複合体を形成し、DNAはヒストン複合体の周囲に巻き付くようにして核内に収納される。ヒストンタンパク質のアミノ酸残基にはさまざまな化学修飾が付加され、これをヒストン修飾という。 - 3.経世代エピゲノム、H3K27me3
H3K27me3はヒストンH3の27番目のリジン残基(K)に三つのメチル基(トリメチル化)が付加したものである。卵のH3K27me3は受精後の着床前発生を通じて維持されたのちに、着床後にはDNAメチル化へと切り替わることで、受精から胎盤発生を通じて母性染色体上の遺伝子の抑制に働く。このように次世代に伝承されるエピゲノムを「経世代エピゲノム」と呼ぶ。 - 4.H2Aub、モノユビキチン
ヒストンH2Aの119番目のリジン残基に一つのユビキチン分子(モノユビキチン)が付加したヒストン修飾で、遺伝子発現の抑制に働く。 - 5.H3K4me3
ヒストンH3の4番目のリジン残基に三つのメチル基が付加したヒストン修飾で、活性化遺伝子マーカーとしてよく知られる。遺伝子発現の促進に働く。 - 6.ゲノム刷り込み
子の遺伝子に父親と母親のどちらの由来の遺伝子であるかが記憶される現象を「ゲノム刷り込み」という。この機構により片親性の遺伝子発現(刷り込み発現)が生じる。マウスにはDNAメチル化依存的な典型刷り込みとH3K27me3依存的な非典型刷り込みの2種類の機構があり、本研究は後者を対象とした研究である。 - 7.微量クロマチン免疫沈降シーケンス法
クロマチンを200~400塩基対(bp)ごとに細断し、特定のヒストン修飾やタンパク質に対する特異的抗体を用いて免疫による抗原抗体反応でクロマチン断片を沈降させる(免疫沈降)。免疫沈降させたクロマチン断片からDNAを抽出し、次世代シーケンサーでその配列を読むことで、ヒストン修飾やタンパク質の結合箇所を同定することができる。研究チームは、100個程度の卵を用いてヒストン修飾の分布を高解像度に同定可能な微量クロマチン免疫沈降シーケンス技術を有する。 - 8.H2Aubを欠損させた卵
H2Aubの付加にはポリコーム抑制複合体1(PRC1:polycomb repressive complex 1)が必須である。PCGF1(polycomb group ring finger 1)とPCGF6(polycomb group ring finger 6)は、PRC1の構成タンパク質の一種であり、卵におけるH2Aubの付与に必須である。H2Aub欠損卵は、PCGF1とPCGF6を欠損させてH2Aubをなくした卵。 - 9.二重欠損卵
卵におけるH3K4me3の付加にはMLL2(myeloid/lymphoid or mixed-lineage leukemia 2)が関与する。H2AubとH3K4me3の両方をなくした二重欠損卵は、PCGF1/6とMLL2を欠損させることで得られる卵。
研究チーム
理化学研究所 生命医科学研究センター
疾患エピゲノム遺伝研究チーム
チームディレクター 井上 梓(イノウエ・アズサ)
研究員 メイ・ハイリャン(Mei Hailiang)
研究員 小塚 智沙代(コヅカ・チサヨ)
テクニカルスタッフⅡ 公文 麻美(クモン・マミ)
免疫器官形成研究チーム
チームディレクター 古関 明彦(コセキ・ハルヒコ)
研究支援
本研究は、日本学術振興会(JSPS)科学研究費助成事業学術変革領域研究(A)「生命を創発する次世代生命工学(領域代表者:高島康弘)」計画研究「エピゲノムによる発生保証機構(研究代表者:井上梓)」、同新学術領域研究(研究領域提案型)「全能性プログラム:デコーディングからデザインへ(領域代表者:小倉淳郎)」計画研究「全能性消失時のエピゲノム制御機構の解明(研究代表者:井上梓)」、基盤研究(B)「卵子の脂質を介した肥満の遺伝機構(研究代表者:小塚智沙代)」、同基盤研究(A)「ポリコムによる分化と共役するゲノム高次構造制御の分子機構解明(研究代表者:古関明彦)」、科学技術振興機構(JST)創発的研究支援事業「ヒストン修飾を基軸とした卵子プログラミング仮説の検証(研究代表者:井上梓)」、日本医療研究開発機構(AMED)革新的先端研究開発支援事業PRIME「経世代ヒストン修飾を介した疾患素因の形成機構(研究開発代表者:井上梓)」、同ムーンショット型研究開発事業「2040年までに、主要な疾患を予防・克服し100歳まで健康不安なく人生を楽しむためのサステイナブルな医療・介護システムを実現」の研究開発プロジェクト「細胞運命転換を用いた若返りによるがんリスク0の世界(研究開発代表者:古関明彦)」、日本応用酵素協会(研究代表者:小塚智沙代)、武田科学振興財団(研究代表者:小塚智沙代)、理研新領域開拓課題「Genome building from TADs(研究代表者:古関明彦、研究分担者:井上梓)」、同「Long-timescale molecular chronobiology(研究代表者:北島智也、研究分担者:井上梓)」による助成を受けて行われました。
原論文情報
- Hailiang Mei, Chisayo Kozuka, Mami Kumon, Haruhiko Koseki, and Azusa Inoue, "H2AK119ub1-MLL2 counteraction underlies heritable H3K27me3 formation in oocytes", Molecular Cell, 10.1016/j.molcel.2026.03.014
発表者
理化学研究所
生命医科学研究センター 疾患エピゲノム遺伝研究チーム
チームディレクター 井上 梓(イノウエ・アズサ)
 井上 梓
井上 梓
報道担当
理化学研究所 広報部 報道担当
お問い合わせフォーム
