理化学研究所(理研)脳神経科学研究センター 知覚運動統合機構研究チームの松田 光司 研究員、久保 郁 チームディレクター、国立遺伝学研究所 比較ゲノム解析研究室の豊田 敦 特任教授、発生遺伝学研究室(研究当時)の川上 浩一 教授(研究当時、現 国立遺伝学研究所 名誉教授)らの共同研究グループは、神経細胞(ニューロン)の活動と遺伝子発現情報を結び付けて解析できる技術「CaMPARI-seq(カンパリシーケンス)」を開発し、動く視覚刺激に対する行動に必要な神経回路を明らかにしました。
本研究成果は、脳での視覚情報の処理や、脳が適切な行動を生み出す過程の理解に貢献するものです。また、「CaMPARI-seq」は神経回路研究の新たな基盤技術となることが期待されます。
視野全体の動きに対する身体の反応は脊椎動物で広く保存されています。しかし、動的な視覚情報が脳内でどのように処理され、その情報に応じて適切な行動がどのように生み出されるのかについては未解明でした。本研究では、ゼブラフィッシュ[1]仔魚(しぎょ)において、開発した「CaMPARI-seq」を用いることにより、動的な視覚情報に反応するニューロンの機能を解析することに成功しました。その結果、動く刺激を感知し、適切な行動を引き起こすのに必須なニューロンを発見しました。
本研究は、科学雑誌『Nature Communications』オンライン版(4月17日付:日本時間4月17日)に掲載されました。
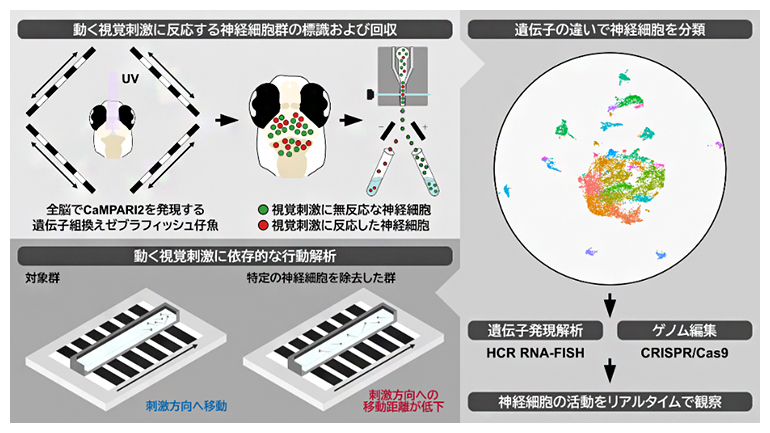
本研究の概要
背景
私たち動物は、目から入る視覚情報を基に、姿勢や視線を適切に保っています。例えば車を運転していると、前の景色が後ろへ流れていくように見えます。私たちはこの見え方を手がかりに速度や距離を感じ取り、ハンドルやブレーキを調節します。また、電車の窓から外を眺めていると、動いている景色を追うように目がゆっくり動いた後に素早く元の位置に戻る動きを繰り返し、視野を安定に保ちます。このような視野全体の動きはオプティックフロー[2]と呼ばれ、オプティックフローに対する身体反応は脊椎動物に広く共通して見られます。しかし、受け取ったオプティックフローが脳内でどのように情報処理され、その情報に応じて適切な行動がどのように生み出されるのか、その詳細な神経回路メカニズムには未解明の点が多く残されています。
オプティックフローには、大きく分けて視野が時計回り・反時計回りに回転する回転性オプティックフローと、前後方向に平行移動する並進性オプティックフローがあり、それぞれ異なる行動を引き起こします。ゼブラフィッシュでは、回転性オプティックフローは主に眼球運動(optokinetic response:OKR)、並進性オプティックフローは遊泳運動(optomotor response:OMR)を誘発します。これまでに、ゼブラフィッシュ仔魚を用いた神経細胞(ニューロン)の活動記録により、前視蓋(ぜんしがい)[3]と呼ばれる脳領域がオプティックフロー情報処理に重要であることが示されています注)。
前視蓋には異なる種類のニューロンが存在することが知られていましたが、これらのニューロンを区別する分子マーカーが不明であったため、特定のニューロンだけを選択的に標識・操作することが困難でした。従来、分子マーカーの同定にはscRNA-seq(1細胞RNAシーケンス)[4]解析が用いられてきました。この手法により、特定の脳領域に含まれる全ニューロンの遺伝子発現情報を網羅的に調べることは可能でしたが、各ニューロンが示す感覚応答といった機能情報と直接対応付けることは困難でした。近年では、活動したニューロンの遺伝子発現を解析する試みは行われつつありますが、解析できるニューロン数は限りがあり、脳全体を網羅的に調べることは困難でした。そのため、前視蓋のどのニューロンがオプティックフローを見分け、どのように異なる行動を生み出しているのかは分かっていませんでした。
そこで共同研究グループは、異なる種類の前視蓋ニューロンを遺伝学的に識別し、それらの機能を解析することのできる新しい手法の開発に挑みました。
- 注)Kubo F, Hablitzel B, Dal Maschio M , Driever W, Baier H, Arrenberg AB., "Functional Architecture of an Optic Flow-Responsive Area that Drives Horizontal Eye Movements in Zebrafish", Neuron, 81, 1344-1359
研究手法と成果
本研究では、オプティックフローに応答する前視蓋ニューロンを標識し、その機能的役割を明らかにするため、新たな解析基盤「CaMPARI-seq」を開発しました。
まず、ほぼ全てのニューロンで核局在型CaMPARI2(カンパリ2)[5]を発現させた遺伝子改変(Tg:Transgenic)ゼブラフィッシュを作製しました。そして、回転性および並進性オプティックフローをTgゼブラフィッシュに提示しながら脳の前視蓋領域にUV(紫外線)光を照射してCaMPARI2の光変換を誘導することにより、オプティックフローに対して活動する細胞を観察しました。その結果、オプティックフローに応答する前視蓋ニューロンを選択的に標識できることを確認しました(図1)。

図1 CaMPARI2によるオプティックフロー応答細胞の標識
(左)オプティックフロー刺激提示下でTgゼブラフィッシュ仔魚にUV光を照射した。(右)オプティックフロー視覚刺激提示後の、Tg(elavl3:NLS-CaMPARI2)遺伝子組換えゼブラフィッシュ仔魚の前視蓋領域の蛍光画像。オプティックフロー反応細胞がCaMPARI2 red(マゼンタ)で標識されている。
次に、オプティックフローに反応したニューロンのみを採取し、scRNA-seq解析を実施しました。得られた30種類のニューロンクラスターについて、既報データを参照して脳領域を絞り込んだ結果、転写因子tcf7l2(transcription factor 7-like 2)遺伝子を発現するクラスターがオプティックフロー応答性ニューロンを豊富に含むことが分かりました。CRISPR/Cas9ゲノム編集技術[6]とカルシウムイメージング[7]を組み合わせた解析により、前視蓋では多数のニューロンがtcf7l2を発現し、これらのニューロンは実際にオプティックフロー刺激に強く応答することを確認しました。このようにして、前視蓋ニューロンの分子マーカーを同定することに成功しました。
さらに、tcf7l2によって特徴付けられる前視蓋ニューロンクラスターを再クラスタリングした結果、七つの前視蓋サブタイプが存在することが判明しました。HCR RNA-FISH[8]による遺伝子発現解析の結果、これらのサブタイプは前視蓋領域において特徴的な遺伝子発現パターンを示し(図2)、解剖学的に異なるサブタイプに対応していることが明らかとなりました。
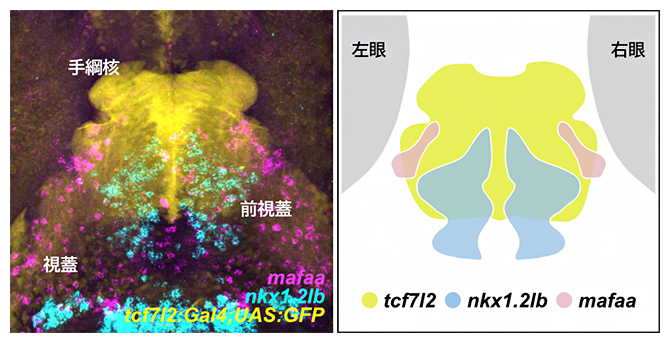
図2 CaMPARI-seqにより同定した前視蓋サブタイプの分布パターン
ゼブラフィッシュ仔魚の前視蓋領域において、転写因子mafaa(MAF bZIP transcription factor Aa)遺伝子と転写因子nkx1.2lb(NK1 transcription factor related 2-like,b)遺伝子の発現をHCR RNA-FISHで可視化した蛍光画像(左)および模式図(右)。前視蓋内では、Tg(tcf7l2-hs:Gal4FF);Tg(UAS:GFP)遺伝子組換えゼブラフィッシュ仔魚の緑色蛍光タンパク質(GFP)陽性細胞(黄色)に加え、mafaa(マゼンタ)およびnkx1.2lb(シアン)の発現が確認される。
さらに、前視蓋において発現分布が異なるこれらの前視蓋サブタイプは、神経投射パターンやオプティックフロー反応パターンにおいても異なるのかを検証しました。その結果、mafaa陽性ニューロンは前視蓋の腹側外側領域に位置する細胞体から局所的に神経突起を伸ばしていました。一方、nkx1.2lb陽性ニューロンは、両半球の脳をつなぐ神経繊維である後交連(こうこうれん)を介して対側の前視蓋へ投射していました。さらに、カルシウムイメージングの結果、mafaa陽性ニューロンは前方から後方への動きに選択的に応答する一方、nkx1.2lb陽性ニューロンは多様なオプティックフロー刺激に広く応答し、複数の反応タイプを含むことが明らかとなりました(図3)。これらの結果から、遺伝子発現プロファイルの異なる前視蓋サブタイプは解剖学的にも機能的にも異なることが明らかになりました。
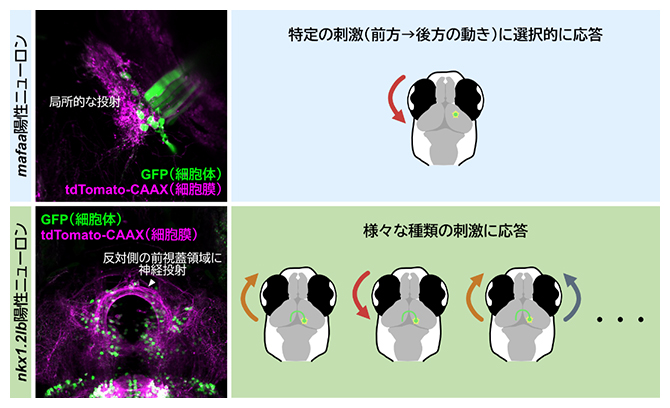
図3 前視蓋サブタイプの形態とオプティックフロー応答特性の違い
- (左)Tg(mafaa-hs:Gal4FF)、Tg(nkx1.2lb-hs:Gal4FF)遺伝子組換えゼブラフィッシュ仔魚において、細胞体をGFPで、細胞膜を赤色蛍光タンパク質のtdTomato-CAAXで標識した蛍光画像。
- (右)オプティックフロー応答特性の概要図。
最後に、これらの前視蓋サブタイプが行動に果たす役割を検証しました(図4)。上述のnkx1.2lb陽性前視蓋ニューロンをニトロレダクターゼ(NTR)/メトロニダゾール(Mtz)システム[9]を用いて特異的に除去したところ、OKRには影響が認められなかった一方で、並進性オプティックフローに依存するOMRは有意に低下しました。自発遊泳には影響が見られなかったことから、基本的な運動能力は維持されていることが確認されました。
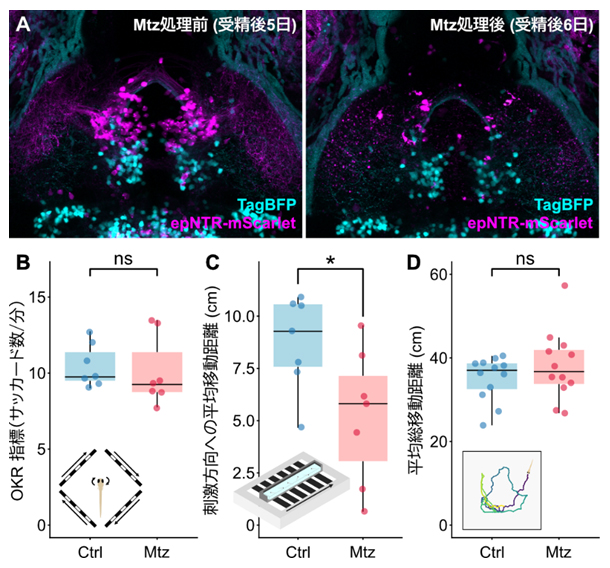
図4 nkx1.2lb陽性前視蓋ニューロンは視運動性の遊泳行動(OMR)に関与
- A.Tg(nkx1.2lb-hs:Gal4FF);Tg(UAS-hs:loxp-TagBFP-loxp-epNTR-mScarlet);Tg(tcf7l2-hs:Cre)遺伝子組換えゼブラフィッシュ仔魚の蛍光画像。nkx1.2lb陽性前視蓋ニューロンでは高活性型ニトロレダクターゼepNTR-mScarlet(マゼンタ)の発現が観察される。メトロニダゾール(Mtz)処理前(左)と比べ、処理後(右)では、nkx1.2lb陽性前視蓋ニューロンのみが特異的に除去されていることが分かる。
- B.対照群(Ctrl)と細胞破壊群(Mtz処理)におけるOKR指標。OKR指標は、サッカード(視線を切り替える際の素早い眼球運動)数の平均として算出した。両群間に有意差は認められなかった(統計手法の一つであるMann-Whitney U検定、ns(not significant(有意差なし))、p(有意水準)=0.4047。
- C.対照群(Ctrl)と細胞破壊群(Mtz処理)におけるOMR時の刺激方向への平均移動距離。対照群の仔魚はしま模様の動く方向へ遊泳したが、Mtz群では遊泳距離が有意に短かった(統計手法の一つであるWelchの2標本t検定、「*」・p<0.05、p=0.03788)。
- D.対照群(Ctrl)と細胞破壊群(Mtz処理)における自発遊泳。90秒間の総移動距離を算出したところ、両群間に遊泳行動に有意な差は見られなかった(Welchの2標本t検定、ns、p=0.3038)。
以上の結果から、nkx1.2lb陽性前視蓋ニューロンは並進性オプティックフローの情報処理に必須である一方、回転性オプティックフローには必須ではないことが明らかとなりました。本研究により、異なるオプティックフロー依存的行動を分離する神経回路の分子基盤が初めて示されました。
今後の期待
本研究で開発したCaMPARI-seqは、神経活動の履歴情報と遺伝子発現プロファイルを全脳スケールで結び付けることを可能にする新規解析基盤です。これにより、特定の機能を持ったニューロン集団の分子プロファイルを体系的に同定することが可能となります。さらに、さまざまな感覚処理や行動制御を担う神経回路の解析に広く応用可能であり、今後は多様な感覚情報処理の仕組みや行動調節への理解が深まることが期待されます。
今後は、異なるサブタイプ間の神経接続や下流運動系神経回路との接続様式の解明を進め、オプティックフロー情報処理を担う神経回路基盤の全体像の解明を目指します。
魚類と哺乳類の脳は基本的な構造や機能において共通性を有しています。本研究で得られた知見は、生体における視覚情報処理の基本原理の解明に貢献するとともに、将来的にはオプティックフローの情報処理原理を取り入れた自動車の自動運転技術の向上などへの波及効果が期待されます。
補足説明
- 1.ゼブラフィッシュ
インド原産の硬骨魚類に属する小型淡水魚(下図)で、飼育が容易かつ多産なモデル実験動物。ゲノム編集などの分子生物学的手法が確立している。ヒトと共通する基本的な脳構造を持ちながら脳が小さく、仔魚ではニューロン数が約10万と少ない。仔魚の脳は透明で、全脳カルシウムイメージング([7]参照)により単一細胞解像度で脳全体の神経活動を非侵襲的に観察できることから、神経回路研究の強力なモデル実験動物となっている。受精後約1週間で視覚依存的な行動を示すため、視覚情報処理に関わる神経回路の解析に適している。

- 2.オプティックフロー
動物が環境内を移動すると、視野全体が自身の動きと逆方向へ流れるように見える。この視覚情報はオプティックフローと呼ばれ、姿勢や眼球運動を調節する感覚情報である。 - 3.前視蓋(ぜんしがい)
前視蓋は間脳の一部で、ゼブラフィッシュでは視蓋の腹側、視床の背側に位置する脳領域である。オプティックフローに応答するニューロンが多く存在し、視運動性眼球反応(OKR)や視運動性遊泳反応(OMR)などの視覚依存的行動に重要な役割を果たす。哺乳類の副視索系に相当する機能を担うと考えられている。 - 4.scRNA-seq(1細胞RNAシーケンス)
個々の細胞における遺伝子発現を網羅的に解析する技術。1細胞ごとにRNA量を定量できるため、細胞ごとの多様性の把握や特異的マーカー遺伝子の同定、これまで検出が困難であった少数の細胞集団の発見が可能となり、組織を構成する細胞タイプや状態を詳細に分類するのに役立つ。 - 5.CaMPARI2(カンパリ2)
CaMPARI(calcium-modulated photoactivatable ratiometric integrator)は、神経活動に伴う細胞内カルシウムイオン(Ca2+)濃度の上昇を利用して活動細胞を標識する蛍光タンパク質。ニューロンが興奮してCa2+濃度が高まった状態でUV光(405ナノメートル(nm、1nmは10億分の1メートル))を照射すると、蛍光が緑色から赤色へ不可逆的に変換される。この性質により、特定の時間窓で特定の感覚刺激に反応したニューロンのみを選択的に標識することができる。本研究では改良型CaMPARIである「CaMPARI2」を使っている。 - 6.CRISPR/Cas9ゲノム編集技術
特定のゲノム配列を狙って改変するゲノム編集技術。ガイドRNAとDNA切断酵素Cas9をゼブラフィッシュ受精卵に導入することで、高効率に遺伝子の欠失や外来遺伝子の挿入(ノックイン)を行うことができる。本研究では、標的遺伝子の転写調節領域にGal4遺伝子をノックインし、遺伝子発現誘導システムであるUASレポーター系統と交配することで、特定の細胞の可視化や操作を可能とするゼブラフィッシュ系統を構築した。 - 7.カルシウムイメージング
神経細胞(ニューロン)が活動すると細胞内カルシウムイオン(Ca2+)濃度が上昇する性質を利用して神経活動を可視化する手法。Ca2+と結合すると蛍光強度が上昇するカルシウムセンサー(例:GCaMP6s)をニューロンに発現させ、その蛍光変化を顕微鏡で観察することで、ニューロンの活動を光として測定できる。これにより、生きた脳内で多数のニューロンの活動を同時に解析することが可能となる。 - 8.HCR RNA-FISH
組織中の特定のRNAの発現場所を高感度に可視化する蛍光in situハイブリダイゼーション法の一つ。HCRはhybridization chain reactionの略。 - 9.ニトロレダクターゼ(NTR)/メトロニダゾール(Mtz)システム
ニトロレダクターゼ(NTR)は、プロドラッグ(生体内の薬剤標的部位での化学反応によって、薬効を示す分子に変換されるようにデザインされた薬剤)であるメトロニダゾール(Mtz)を細胞毒性化合物へと変換する酵素である。この酵素を発現する細胞にMtzを投与するとDNA損傷が引き起こされ、その細胞のみが選択的に死滅する。本研究では、Cre-loxPシステム(細胞種選択的に遺伝子発現を操作する遺伝子工学技術の一つ)と組み合わせることで、前視蓋に位置するnkx1.2lb陽性ニューロンに特異的に高活性型NTR(epNTR)を発現させ、Mtz投与によりこれらのニューロンを選択的に除去した。
共同研究グループ
理化学研究所 脳神経科学研究センター
知覚運動統合機構研究チーム
研究員 松田 光司(マツダ・コウジ)
研修生 チョンハン・ワン(Chung-Han Wang)
(総合研究大学院大学 遺伝学コース 5年一貫制博士課程5年)
テクニカルスタッフⅠ 柿沼 久哉(カキヌマ・ヒサヤ)
チームディレクター 久保 郁(クボ・フミ)
国立遺伝学研究所
比較ゲノム解析研究室
特任教授 豊田 敦(トヨダ・アツシ)
発生遺伝学研究室(研究当時)
特任助教(研究当時)白木 知也(シラキ・トモヤ)
(現 労働安全衛生総合研究所 任期付研究員)
教授(研究当時、現 国立遺伝学研究所名誉教授)川上 浩一(カワカミ・コウイチ)
研究支援
本研究は、日本学術振興会(JSPS)科学研究費助成事業研究活動スタート支援「視覚情報の統合を司るゼブラフィッシュ前視蓋における階層的な神経回路基盤(研究代表者:松田光司)」、同若手研究「視覚刺激応答細胞の標識と1細胞RNA-seqによる前視蓋神経回路の形態・機能解析(研究代表者:松田光司)」「前視蓋神経細胞サブタイプの遺伝学的分類による視覚情報処理メカニズムの解析(研究代表者:松田光司)」、同基盤研究(B)「トランスポゾンを用いた遺伝子トラップ法に基づく生命科学の基盤形成(研究代表者:川上浩一)」「視覚情報処理ネットワークの広範な活性化を駆動するハブ神経回路の解析(研究代表者:久保郁)」、同国際共同研究加速基金(帰国発展研究)「視覚情報処理と行動制御の基盤となる神経メカニズムの解明(研究代表者:久保郁)」、同国際共同研究加速基金(国際先導研究)「記憶メカニズムの多次元解析-nmからメゾスケール/ミリ秒から日スケールまで(研究代表者:林康紀)」、情報・システム研究機構戦略的研究プロジェクト「脊椎動物ゼブラフィッシュを利用した多感覚情報を統合する脳地図データベースの構築(研究代表者:松田光司)」、日本分子生物学会若手研究助成富澤純一・桂子基金「視覚情報処理を制御する神経回路の機能と結合様式の解明(研究代表者:久保郁)」による助成を受けて行われました。
原論文情報
- Koji Matsuda, Chung-Han Wang, Hisaya Kakinuma, Atsushi Toyoda, Tomoya Shiraki, Koichi Kawakami, Fumi Kubo, "Molecular and functional dissection using CaMPARI-seq reveals the neuronal organization for dissociating optic flow-dependent behaviors", Nature Communications, 10.1038/s41467-026-71371-6
発表者
理化学研究所
脳神経科学研究センター 知覚運動統合機構研究チーム
研究員 松田 光司(マツダ・コウジ)
チームディレクター 久保 郁(クボ・フミ)
国立遺伝学研究所
発生遺伝学研究室(研究当時)
教授(研究当時、現 国立遺伝学研究所名誉教授)川上 浩一(カワカミ・コウイチ)
比較ゲノム解析研究室
特任教授 豊田 敦(トヨダ・アツシ)
 松田 光司
松田 光司
 久保 郁
久保 郁
報道担当
理化学研究所 広報部 報道担当
お問い合わせフォーム
国立遺伝学研究所 広報室
Email: prkoho@nig.ac.jp
