理化学研究所(理研)脳神経科学研究センター 学習・記憶神経回路研究チームのジョシュア・ジョハンセン チームディレクター、植松 朗 研究員(研究当時)らの共同研究グループは、ラットにおいて嫌悪記憶が想起された際に、脳が記憶を「再固定化する」神経回路メカニズムと分子機構を明らかにしました。
本研究成果は、心的外傷後ストレス障害(PTSD)[1]などにおいて恐怖などの嫌悪記憶が過度に強化されるメカニズムの理解に貢献することが期待されます。
共同研究グループは、ラットが嫌悪記憶を想起する際の脳の青斑核(せいはんかく)[2]におけるノルアドレナリン作動性ニューロン[3]の活動が、記憶の再固定化の中心的役割を担うことを見いだしました。嫌悪記憶の想起に伴って青斑核からノルアドレナリン[3]が放出され、扁桃体の外側核・基底外側核(LA/B)から中央核(CeA)へ投射[4]するニューロンに存在するβ2アドレナリン受容体[5]を介して再固定化すること、このノルアドレナリンのシグナルにより転写因子コアクチベーターCRTC1[6]を介して再固定化に必要な遺伝子発現を誘導すること、さらに嫌悪記憶の想起直前のストレスにより再固定化された記憶が強化されるメカニズムを明らかにしました。
本研究は、科学雑誌『Neuron』オンライン版(3月3日付:日本時間3月4日)に掲載されました。
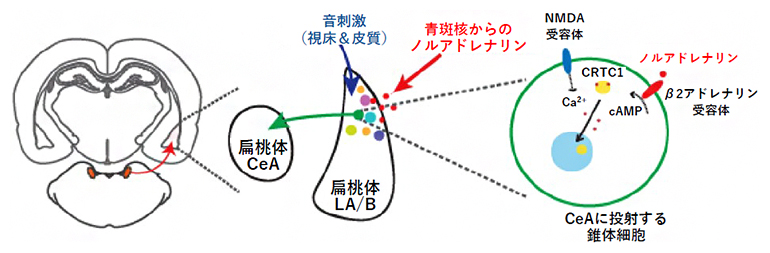
嫌悪記憶の再固定化に関わる脳回路
背景
記憶は固定されているように見えますが、実際には想起するたびに一時的に不安定化し、その後再び固定化(再固定化)されて、最新情報に基づく更新・再編が行われます。記憶の再固定化により、脳は柔軟に記憶の強弱や内容を変化させて、新しい環境へ適応したり、記憶を更新したり、不要な記憶を整理したりできます。
例えば、スズメバチに刺される恐怖体験をした場合、その場所を記憶して回避することは、動物が生き延びるために重要です。しかし、その後スズメバチが駆除されて環境が変わり、その場所での楽しい体験が積み重なれば、恐怖体験の記憶が再編されて新しい環境へ適応できます。一方、難しい試験の前などのストレスを感じた状態で、スズメバチに刺された恐怖体験を思い出すと、恐怖体験の記憶が強化されてスズメバチに対する嫌悪感が強まって更新されます。
このような現象は広く知られているものの、その背後にある神経回路や分子機構は十分に理解されていませんでした。
また、恐怖体験などの嫌悪記憶は脳の扁桃体で形成されて保存されること、一度保存された嫌悪記憶の再固定化にはストレスホルモンであるノルアドレナリンとその受容体が関わることが先行研究から示唆されています注)。しかし、どの神経回路が活性化され、どの細胞集団で記憶の更新に必要な遺伝子発現が制御されるのかは不明でした。
脳内で作用するノルアドレナリンは、そのほとんどが脳幹の青斑核から投射するノルアドレナリン神経群から放出されます。そこで、共同研究グループは、嫌悪記憶の想起時における記憶の再固定化に青斑核の活動が必要かどうかを、ラットを用いて光遺伝学法[7]により調べました。
- 注)Dissruption of reconsolidation but not consolidation of auditory fear conditioning by noradrenergic blockade in the amygdala , J Debiec and JE Ledoux, Neuroscience 2004; 129(2):267-272, 10.1016/j.neuroscience.2004.08.018
研究手法と成果
まず、ラットに嫌悪記憶を記憶させて、想起後の再固定化の際に、青斑核ニューロンの活動を光遺伝学法により制御して、青斑核の活動と嫌悪記憶の再固定化との関係を調べました(第1の実験)。
ラットに音刺激と電気刺激を同時に与えると、二つの刺激が連合されて嫌悪記憶が形成され、音刺激だけを与えても恐怖反応であるすくみ反応[8]を示すようになります。ラットに表出するすくみ反応の時間により、嫌悪記憶の想起や再固定化を評価できます。まず、ラットに音刺激と電気刺激を同時に与えることを3回繰り返して嫌悪記憶として記憶させました(恐怖条件付け)。次に、4週間後に嫌悪記憶を想起させる合図となる音刺激だけを提示して、音刺激と連合した電気刺激の嫌悪記憶を想起させました(記憶想起)。さらに、1日後に音刺激を提示して嫌悪記憶を再固定化させました(再固定化)。嫌悪記憶を想起させる音刺激の提示中だけ扁桃体のLA/Bに結合する青斑核ニューロンの神経末端に光を当てて、青斑核ニューロンの活動を光遺伝学法により抑制したラットを光遺伝学群のラットとしました(図1a)。音刺激提示以外のタイミングで光を当てたラットを光遺伝学対照群のラット、光照射をしなかったラットを対照群ラットとしました。
恐怖条件付けや記憶想起では、光遺伝学群と対照群とで差はありませんでしたが、光遺伝学群において再固定化が起こっていませんでした(図1b)。この結果から、青斑核の活動は再固定化に特異的に必要であることが分かりました。
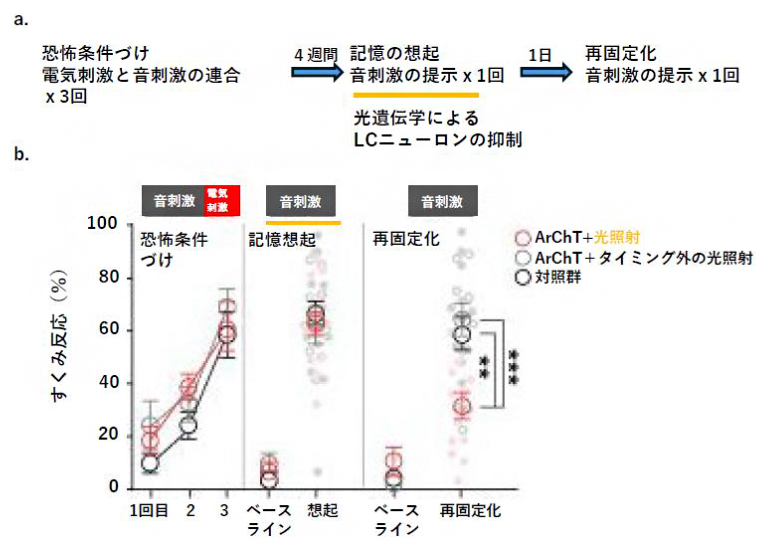
図1 青斑核ニューロンは記憶の再固定化に必要
- a.実験スケジュール。音刺激と軽い電気刺激を同時に3回繰り返し与えて(恐怖条件付け)、4週間後に音刺激だけを提示して(記憶想起)、更に1日後に音刺激を提示した(再固定化)。光遺伝学群については、嫌悪記憶を想起させる際、音刺激の提示と同時に光遺伝学法により青斑核(LC)ニューロンの活動を抑制した。
- b.縦軸はラットがすくみ反応を見せた時間の割合(%)。音刺激と電気刺激の連合を3回繰り返して与えるとすくみ反応は光遺伝学群(赤抜き丸)、光遺伝学対照群(灰抜き丸)、対照群の(黒抜き丸)の全てで増加し、4週間後でも音刺激の提示によりラットは同程度のすくみ反応を示し、嫌悪記憶を想起したことを確認した。光遺伝学群(赤抜き丸)においては音刺激提示に合わせて光照射によって青斑核ニューロンの活動を抑制し、光遺伝学対照群(灰抜き丸)においては音刺激提示以外のタイミングで光照射によって青斑核ニューロンの活動を抑制した。いずれの群でも音刺激に対して光照射を行わない対照群(黒抜き丸)と同程度すくみ反応を示し、記憶想起に問題がないことが確認された。しかし、さらに1日後に音刺激を提示したところ、光遺伝学群(赤抜き丸)においては、すくみ反応が減少し嫌悪記憶の再固定化が起こっていないことが分かった。光遺伝学対照群(灰抜き丸)および対照群(黒抜き丸)では、恐怖条件付け、記憶想起の時と同程度のすくみ反応を示した。「**」有意水準1%での有意差あり、「***」有意水準0.1%での有意差あり。
次に、恐怖やストレスに関連する記憶の固定化と情動反応の制御において、中心的な役割を果たしている扁桃体LA/Bにおけるβ2アドレナリン受容体と、嫌悪記憶の再固定化との関係を調べました。特定のLA/Bニューロンでβ2アドレナリン受容体の発現をノックダウンしたラットをβアドレナリン受容体ノックダウン群として対照群と比較しました(図2a、第2の実験)。実験スケジュールは第1の実験と同じです。
恐怖条件付けや記憶想起では、βアドレナリン受容体ノックダウン群と対照群とで差はありませんでした。再固定化においては、βアドレナリン受容体ノックダウン群でのみ、顕著にすくみ反応時間が減少し、再固定化が阻害されていることが確認されました(図2b)。
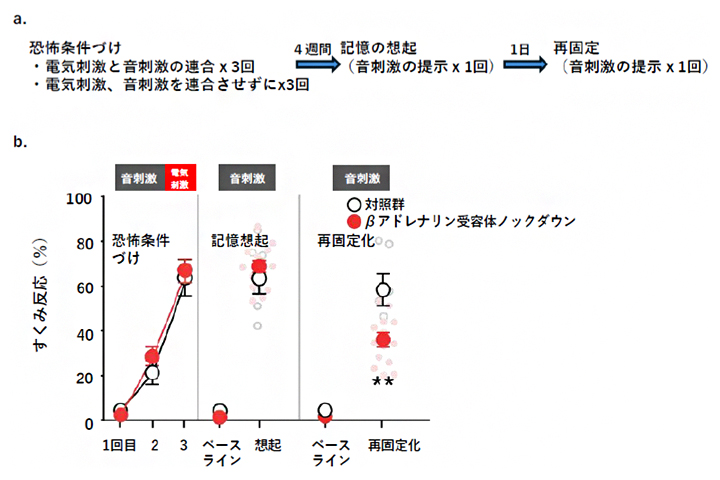
図2 βアドレナリン受容体は再固定化に必要
- a.実験スケジュール。音刺激と軽い電気刺激を同時に(連合)与えることを3回繰り返し与えた。4週間後に音刺激だけを提示して、電気刺激による嫌悪記憶を想起するかどうかを確認した。さらに1日後に再び音刺激を提示し、嫌悪記憶が再固定化するかどうかを確認した。対照群では、電気刺激と音刺激をバラバラ(非連合)に与えることを3回繰り返した。同様に4週間後に音刺激を提示して記憶想起を確認し、さらに1日後に音刺激を提示して嫌悪記憶の再固定化を行った。
- b.縦軸はラットがすくみ反応を見せた時間の割合(%)。音刺激と電気刺激を3回繰り返すと扁桃体LA/Bにおけるβアドレナリン受容体ノックダウン群(赤丸)、対照群(黒抜き丸)の両方ですくみ反応が増加し、4週間後でも音刺激の提示により嫌悪記憶の想起が確認された。しかし、さらに1日後に音刺激の提示により再固定化を試みると、扁桃体LA/Bにおけるβアドレナリン受容体ノックダウン群(赤丸)でのみ顕著にすくみ反応が減少し、再固定化の阻害が確認された。「**」有意水準1%での有意差あり。
長期記憶の形成には、特定の遺伝子発現が必要です。遺伝子発現の制御においては一般に目的の遺伝子上に転写因子が結合することで遺伝子の転写が開始します。転写因子と結合して遺伝子の転写率を高める転写因子コアクチベーターCRTC1(以下「CRTC1」)は、神経活動依存的に細胞核に移行し記憶固定化に関わることから注目しました。
共同研究グループは、ラットに音刺激と電気刺激を連合して与えてから29日後に音刺激のみを提示して嫌悪記憶を想起させ、扁桃体LA/B組織におけるCRTC1の局在を免疫染色法を用いて観察しました。対照群としては、音刺激と電気刺激を連合して与えてから29日後に同じケージに入れたラットと、音刺激と電気刺激を別々に与え(非連合)てから29日後に音刺激のみを提示したラットの扁桃体LA/B組織におけるCRTC1の局在を同様に免疫染色法を用いて観察しました。その結果、記憶想起時にCRTC1が扁桃体LA/Bニューロンの細胞質から細胞核へ迅速に移行することを発見しました(図3a、b)。CRTC1は核内で標的遺伝子の転写を促進し、標的遺伝子の発現を増加させます。つまり、記憶想起によりCRTC1を介して標的遺伝子発現を促進することが示唆されました。この現象は、音刺激と電気刺激を連合して与え、その後の記憶を想起した場合にのみ生じましたが、音刺激と電気刺激を非連合で与えた場合には生じませんでした。さらにCRTC1をノックダウンして阻害すると再固定化だけが障害されることから、CRTC1が再固定化を行う因子であることが明らかになりました。
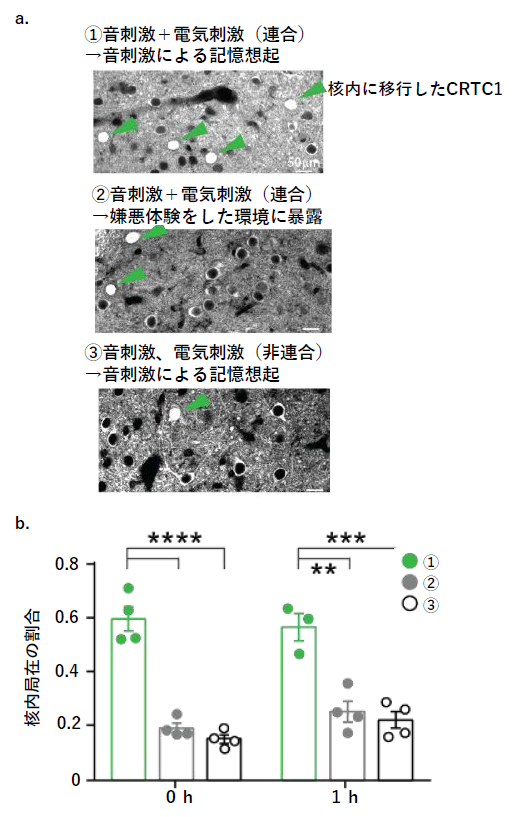
図3 記憶想起特異的にCRTC1の核内移行が増加
- a.扁桃体LA/B組織のCRTC1免疫染色。CRTC1が存在している細胞核は画像処理により白く標識されている(緑矢じり)。①音刺激と電気刺激を連合して与え、29日後に音刺激を提示して記憶を想起させた場合、②音刺激と電気刺激を連合して与え、29日後に同じ実験環境を提示するだけで記憶を想起させない場合、③音刺激と電気刺激を非連合し、29日後に音刺激を提示した場合、の三つの条件を比較すると①における扁桃体LA/BニューロンにおいてCRTC1(緑矢じり)の核内移行が多く見られた。スケールバーは50マイクロメートル(μm、1μmは100万分の1メートル)
- b.a.の実験の定量評価。①音刺激と電気刺激を連合して与え、29日後に音刺激を提示して記憶を想起させた場合(緑丸)においてのみ、音刺激提示直後(0h)からCRTC1の核内局在の割合が高くなっており、さらにその1時間(1h)後でも核内局在割合は高いままであった。「**」有意水準1%での有意差あり、「***」有意水準0.1%での有意差あり、「****」有意水準0.01%で有意差あり。
共同研究グループはまた、青斑核ニューロンの活動とβ2アドレナリン受容体シグナルがCRTC1の核移行に不可欠であることを示しました。青斑核からの投射ニューロンを阻害した場合や、β2アドレナリン受容体をノックダウンした場合には、扁桃体LA/BニューロンにおけるCRTC1の核移行が見られませんでした。これらの結果から、青斑核ニューロンが活性化すると、β2アドレナリン受容体シグナルを介してCRTC1が活性化され、記憶の再固定化を促進するという因果関係を明らかにしました。
最後に共同研究グループは、記憶の再固定化に対するストレスの影響を調べました。その結果、記憶想起前の軽度なストレスが再固定化を強化すること、また、光で活性化するβ2アドレナリン受容体シグナルを発現させた上で光を当て活性化するだけで同様の強化が生じることを示しました。
今後の期待
本研究は、記憶の再固定化を制御する脳の回路から受容体、そして核内シグナルへと至る一連の仕組みを初めて包括的に示すものです。本研究の成果は、PTSDや不安障害のように嫌悪記憶が過度に強く、持続的に形成される疾患の理解と治療法開発に大きく貢献すると期待されます。今後は、β2アドレナリン受容体やCRTC1経路を標的とした新規治療法の開発や、ストレスによる記憶強化を防ぐ心理的介入アプローチなどへの展開が期待されます。
補足説明
- 1.心的外傷後ストレス障害(PTSD)
生命を脅かすような非常に強い恐怖などの嫌悪記憶が残り、何げない状況でも嫌悪記憶がフラッシュバックすることにより、日常生活に支障を来してしまう障害。PTSDはPost-Traumatic Stress Disorderの略。 - 2.青斑核(せいはんかく)
脳幹の橋上部背側にあるノルアドレナリン作動性ニューロン([3]参照)の主要核。青味がかるように見えるためこのような名称が付いている。 - 3.ノルアドレナリン作動性ニューロン、ノルアドレナリン
ノルアドレナリンは化学式C8H11NO3のカテコールアミンであり、ノルエピネフリンとも呼ばれるストレスホルモンの一種である。交感神経を活性化し、心拍数を増加させる他、長期記憶の形成などにも関与する。ノルアドレナリンを放出するニューロン(神経細胞)をノルアドレナリン作動性ニューロンと呼ぶ。 - 4.扁桃体の外側核・基底外側核(LA/B)から中央核(CeA)へ投射
嫌悪記憶形成と恐怖反応の表出を担う扁桃体の主要経路。 - 5.β2 アドレナリン受容体
ノルアドレナリンを受容するGタンパク質(グアニンヌクレオチド結合タンパク質の総称)共役受容体。 - 6.転写因子コアクチベーターCRTC1
神経活動依存的に遺伝子発現を制御する転写共役因子。 - 7.光遺伝学法
光で活性化されるイオンチャネルやイオンポンプを神経細胞に発現させ、青色光や緑色光を照射することで、その神経細胞の活動を活性化したり抑制したりする技術。 - 8.すくみ反応
動物の恐怖反応の一つで、体を動かさずにしばらくじっとしている行動。
共同研究グループ
理化学研研究所 脳神経科学研究センター 学習・記憶神経回路研究チーム
チームディレクター ジョシュア・ジョハンセン(Johansen Joshua)
(東京大学大学院総合文化研究科 客員教授)
研究員(研究当時)タン・バオ・ゼン(Bao Zhen Tan)
テクニカルスタッフⅠ 吉田 玲子(ヨシダ・レイコ)
研究員(研究当時)植松 朗(ウエマツ・アキラ)
(現 産業技術総合研究所 主任研究員、東京大学大学院農学生命科学研究科 応用動物科学専攻 准教授)
リサーチアソシエイト(研究当時)
ジェニー・コイヴマー(Jenny Koivumaa)
東京大学大学院農学生命科学研究科 応用動物科学専攻
博士課程(研究当時)ジェシカ・ナタリ・サルケス・クエバス(Jessica Natali Sulkes Cuevas)
沖縄科学技術大学院大学(OIST)シナプス生物学ユニット
教授 合田 由紀子(ゴウダ・ユキコ)
研究支援
本研究は、日本学術振興会(JSPS)科学研究費助成事業若手研究(A)「青斑核ノルアドレナリン神経の多様性を生み出す機構の解明(研究代表者:植松朗)」、同新学術領域研究(研究領域提案型)「Noradrenergic regulation of fear and extinction learning(研究代表者:ジョシュア・ジョハンセン)」「Circuit based genome editing for the treatment of stress related psychiatric disorders(研究代表者:ジョシュア・ジョハンセン)」、同基盤研究(B)「Dopaminergic regulation of fear extinction learning(研究代表者:ジョシュア・ジョハンセン)」、同若手研究(B)「Neural circuit and molecular mechanisms for noradrenergic modulation of fear learning and memory(研究代表者:タン・バオ・ ゼン)」による助成を受けて行われました。
原論文情報
- Bao Zhen Tan*, Jessica Natali Sulkes Cuevas*, Reiko Yoshida*, Akira Uematsu, Jenny Koivumaa, Yuri Ishizu, Yukiko Goda, Joshua P. Johansen, "A neuromodulatory circuit-to-molecular pathway for reformatting aversive memories during recall", Neuron, 10.1016/j.neuron.2026.01.006
発表者
理化学研究所
脳神経科学研究センター 学習・記憶神経回路研究チーム
チームディレクター ジョシュア・ジョハンセン(Johansen Joshua)
研究員(研究当時)植松 朗(ウエマツ・アキラ)
 ジョシュア・ジョハンセン
ジョシュア・ジョハンセン
報道担当
理化学研究所 広報部 報道担当
お問い合わせフォーム
