2026年3月27日
理化学研究所
慶應義塾大学
科学技術振興機構(JST)
脂質を包括的に可視化する新たな空間解析手法の開発
-多層的な質量分析イメージングで脂質の空間制御の解明に貢献-
理化学研究所(理研)生命医科学研究センター メタボローム研究チームの内野 春希 特別研究員、津川 裕司 客員研究員、有田 誠 チームディレクター(慶應義塾大学 薬学部・薬学研究科 教授)の研究チームは、生体組織内の脂質分子を包括的かつ詳細に可視化する質量分析イメージング(MSI)[1]の新手法「SMASH imaging(Serial MAldi-ms Strategy for High-resolution imaging)」を開発しました。
本研究成果は、脂質イメージングの網羅性と構造解析の正確性を向上させ、脂質分布の空間地図(リピドームアトラス)の構築を通じて、脂質が関与する加齢・発生・神経疾患・がんなどの生命現象や、病気の解明へ貢献することが期待されます。
従来の質量分析イメージング手法では、十分な分子情報を得るためには何度もレーザー照射が必要であるため、照射によって試料が消失し、同じ場所での連続計測は困難でした。つまり、計測回数が制限されるため1枚の組織から多様な脂質分子の空間地図を描くことは困難でした。本手法は、イオンを一時的に蓄積・濃縮してから分離するイオンモビリティー[2]技術を活用することで、従来の10分の1という少ないレーザー照射回数でも必要な分子情報を得ることを可能にしました。また、従来の分析技術で得られた脂質プロファイルの結果と比較することで、本手法で得られる脂質分布の正確性を確認しました。さらに、1枚の組織切片の同じ場所で4回から12回の連続計測を実現し、マウスの脳組織切片1枚から400種類以上の脂質分子の分布を詳細に把握することに成功しました。
本研究は、科学雑誌『Analytical Chemistry』オンライン版(3月26日付:日本時間3月27日)に掲載されました。
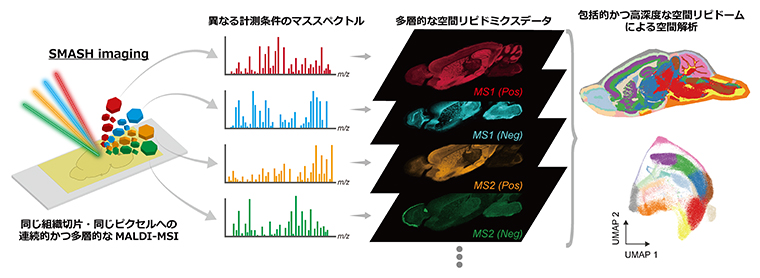
新手法SMASH imagingによって脂質分布の空間地図(リピドームアトラス)を構築
背景
脂質は細胞膜の主要構成要素であり、エネルギー代謝、細胞内外のシグナル伝達、バリア機能など多岐にわたる生命活動を支える必須分子です。脂質は非常に多様な分子構造を持ち、それぞれの臓器や細胞の種類に応じた特徴的な脂質環境を形成することで、生体の機能が維持されていると考えられています。質量分析を用いて多種多様な脂質の量と質(分子構造)を解析するリピドミクスは、これまでに正常な組織や細胞が持つ脂質環境を捉えるとともに、さまざまな疾患の解析を通じて脂質代謝ネットワークの変化と破綻への道筋が解き明かされてきました。近年の質量分析によるリピドミクス研究を通じて、老化・がん・動脈硬化・神経変性疾患など多岐にわたる疾患での脂質の変動と役割が解明されつつあります。
一方で、これまでに広く行われてきたリピドミクスは、検体をすりつぶして計測する組織全体の解析(バルク解析)であるため、どんな脂質がどの組織部位や細胞の中で空間的に分布しているのかについてはその多くが分かっていません。この未開拓な脂質の空間地図(リピドームアトラス)を解明することは、リピドミクスが貢献してきた脂質の関わる生物学や疾患の病態解明をさらに推し進める重要な情報および技術基盤となります。しかし、「どこに、どんな脂質分子が存在するか」という生体内の脂質分子の分布情報(空間リピドーム)を「網羅的」かつ「分子構造の確からしさ」を両立して明らかにすることは容易ではありません。脂質分子は正負どちらのイオンになりやすいかの傾向が異なるため、脂質の質量分析には、正負両方のイオンモードで計測することが求められます。また脂質は構造多様性を持つため、基本骨格・極性基・アシル基などの部分構造を詳しく知るためにタンデム質量分析[3]を用いたMS/MSスペクトル[4]が必要です。つまり、脂質の空間地図を解明するためには、種々の質量分析データ(マススペクトル)を空間解析で計測することが欠かせません(図1)。
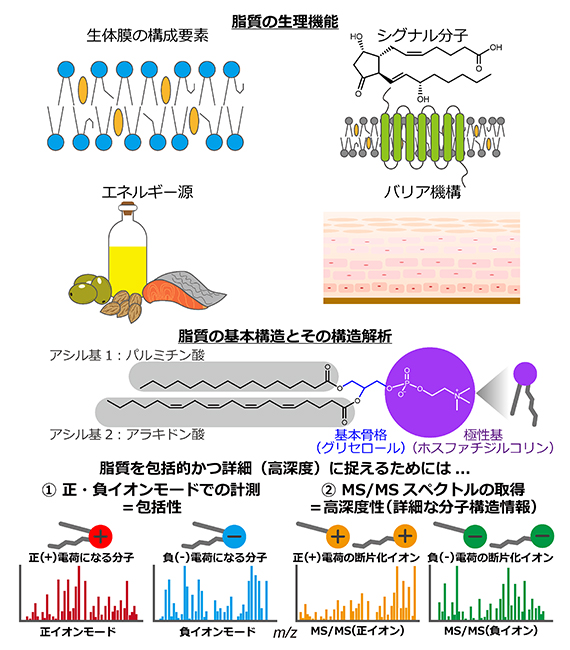
図1 脂質の生理機能と質量分析を用いた脂質の構造解析(リピドミクス)
- (上) 脂質は生体膜の構成要素であるとともに、エネルギー源、細胞内外のシグナル伝達分子、バリア機能など生命活動を支える必須の分子である。
- (下) 正イオン・負イオンモードでの異なる質量分析(①)やタンデム質量分析を用いたMS/MSスペクトル(②)など種々の質量分析データを取得する必要がある。
近年、マトリックス支援レーザー脱離イオン化法(MALDI)[5]-質量分析イメージング(MSI)(MALDI-MSI)により組織切片上の脂質分布を可視化する「空間リピドミクス」が発展しています。しかし、従来法では十分なイオンを得るために1度の計測点(ピクセル)に対してUV(紫外線)レーザーを数百回も照射するため、サンプル上のマトリックス結晶[6]が消失し、同じ検体の同じピクセルで別のマススペクトルを新たに測定することは困難でした。そのため、従来は複数枚の連続切片を用いたり、解像度を犠牲にした工夫(ピクセルを飛び飛びに計測して異なるマススペクトルを取得する一方で、各マススペクトルを統合した最終的なピクセルサイズが大きくなってしまう手法)をしたりしていました(図2)。
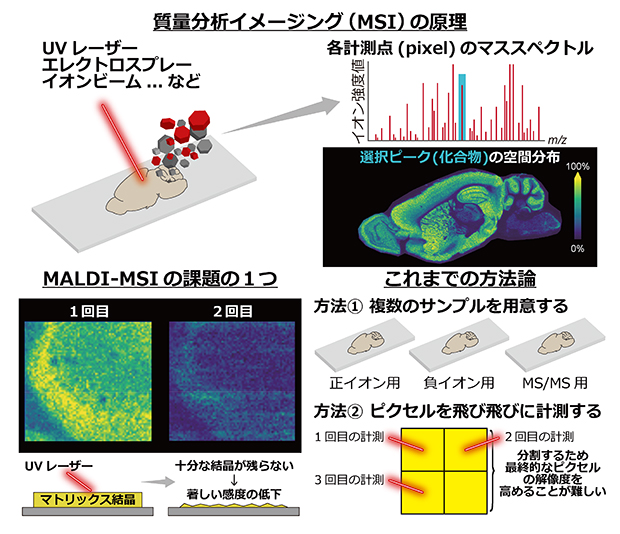
図2 質量分析イメージングの原理とMALDI-MSIの課題
- (上) 質量分析イメージング(MSI)の原理:質量分析イメージング(MSI)は組織切片にUVレーザーなどを照射して、各ピクセルのマススペクトルを取得し、脂質の空間分布を可視化する。
- (下左) MALDI-MSIの課題の一つ:従来のMALDI-MSIは、同じ検体の同じピクセルで別のマススペクトルを新たに測定することは困難だった。
- (下右) これまでの方法論:①複数のサンプルを用意する(上)や②ピクセルを飛び飛びに計測する(下)、という方法が取られていた。
研究手法と成果
本研究では、同じ組織切片上の同じピクセルを繰り返し測定しながら多層的なマススペクトルデータを取得するために、質量分析と併用されるイオンモビリティー技術の一種である「Trapped ion mobility spectrometry(TIMS)」の特性に着目しました。TIMSは一時的にイオンを蓄積・濃縮してから分離する仕組みを持ち、少ないイオンをまとめて検出することで感度向上が期待されます。研究チームは、このTIMSを利用することで、通常のUVレーザー照射数よりも10分の1という少ない回数で必要なイオンシグナルを得られることを示しました(図3a、b)。
さらに、何回まで連続測定が成立するのかを評価するため、各測定回におけるイオン強度値の再現性から決定係数(R2:検量線の直線性を示す指標)を算出し、可能な連続計測数を定量的に定義しました。この評価指標を用いて、マトリックスの種類、マトリックス塗布量の厚さ、レーザー照射条件などを異なる条件因子を組み合わせながら評価しました。その結果、特性の異なる二つのマトリックス化合物が、SMASH imagingに適していることを見いだし、現在の市販装置の最高解像度(5マイクロメートル(μm、1μmは100万分の1メートル))を含めた条件で4~12回の連続計測が可能であることを示しました(図3c)。
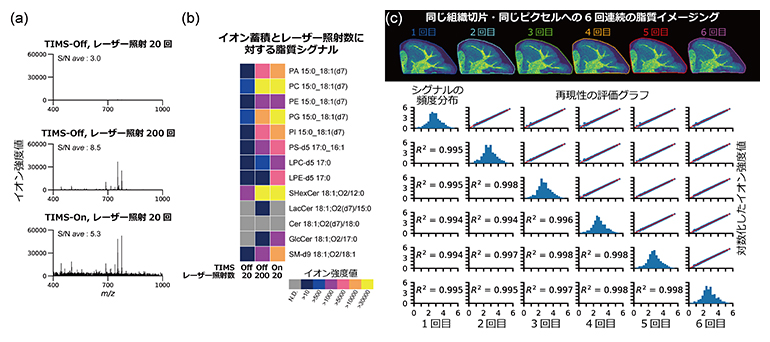
図3 SMASH imagingの研究開発
- (a)イオン蓄積(TIMS)の有無(On・Off)とUVレーザー照射数別のマススペクトル。TIMS-Onでは10分の1のレーザー照射数(20回)でもTIMS-Off時のレーザー照射数(200回)と同程度のイオン強度値が得られることが分かった。
- (b)TIMSの有無とレーザー照射数に対する脂質シグナル強度の結果。各種の脂質標準品を用いて評価している。
- (c)SMASH imagingできる計測回数の評価例。
本手法で得られる脂質分布の妥当性を検証するため、レーザーマイクロダイセクション[7]で採取したマウス小脳の白質・顆粒層・分子層の3層のサンプルを液体クロマトグラフィータンデム質量分析(LC-MS/MS)[8]で計測し、本手法の結果と比較しました。その結果、両手法で得た脂質プロファイルは各層構造ごとに高い相関性を示したことから、SMASH imagingで可視化された脂質分子の空間情報の確からしさが確認されました。
最適化した条件下でマウス脳を計測すると、正・負の両イオンモードにおいて30μm解像度では平均400種類、5μm解像度ではおよそ90種類の脂質分子を構造解析(構造アノテーション)しました(図4a)。MSIにおける分子構造アノテーションは、通常、質量情報(質量電荷比:m/z)のみで行われることが一般的ですが、本研究ではマウス脳のLC-MS/MS解析で得た脂質プロファイルからデータベースを構築し、m/z・イオンモビリティー移動度(1/K0)・S/N比(Signal-to-Noise ratio:信号対ノイズ比)の多角的な基準を基に、正確性を向上した構造アノテーションを実施しました。400種以上のアノテーション数は、組織全体の解析(バルク解析)で捉えられる数の60%以上をカバーしており、空間解析としての包括性が飛躍的に向上しました。さらに、従来は1枚の切片から一つのターゲット分子のMS/MSスペクトルを取得していましたが、SMASH imagingでは可視化できた分子のうち20~30種類をターゲットとして連続的にMS/MSスペクトルが取得できるようになり、側鎖異性体[9]を含めたさらに詳細な構造アノテーションと空間分布が判明しました(図4c)。
また、質量分析イメージングの情報科学「MSIインフォマティクス」の観点において、SMASH imagingは各種マススペクトルを内包した高次元データ解析(UMAP[10]や空間クラスタリングなど)やプリカーサーイオンとそのフラグメントイオン[11]との共局在性解析などを実施できる点で大きな進歩性があります。同じピクセルでの計測の利点を活かした空間クラスタリングを行うことで、正負の両イオンモードから検出される多様な脂質分布を全て加味した脂質分布のパターン把握できるようになりました。また、タンデム質量分析で課題となるターゲット分子以外の分子が取得データに紛れ込む問題についても、プリカーサーイオン(ターゲット分子)と断片化イオンの共局在性(統計的に評価可能な指標)を設定し評価することで、解析に値する断片化イオン(空間共局在の高い断片化イオン)を抽出可能であるという方法論を初めて示しました。以上のようにSMASH imagingだからこそ実現可能な発展的なMSIデータ解析についても、その実用性が示されました(図4b)。本手法は、各種マススペクトルを連続的・多層的に取得するその包括性および高深度性から、空間リピドミクスをさらに進展させる技術になると考えられます。
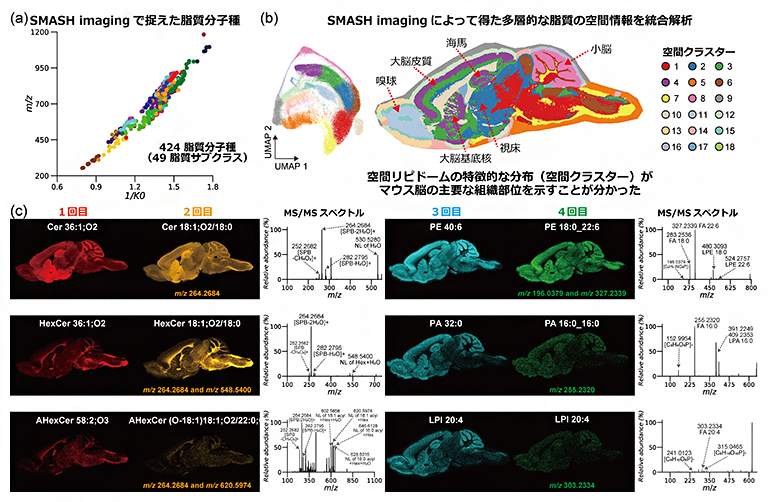
図4 マウス脳のSMASH imaging
- (a)SMASH imagingでアノテーションされた脂質分子種の質量電荷比(m/z)とイオンモビリティー移動度(1/K0)の散布図。
- (b)SMASH imagingデータを用いたUMAPおよび空間クラスタリングの結果。
- (c)SMASH imaging(4回計測)で得られた多層的なMSIデータ(脂質イメージング像およびMS/MSスペクトル)の例。
以上より、本手法は同一切片・同一ピクセルから高解像度に各種マススペクトルを取得できる実用的かつ革新的な手法であることが実証されました。
今後の期待
本研究で開発したSMASH imagingは、可視化できる脂質・代謝物の数と構造アノテーションの精度・深度を向上したことに加えて、同一組織・同一ピクセル上で異なるマススペクトルデータを連続取得できることを実証した点に本質的な意義があります。これは、LC-MS/MSなどでData Dependent Acquisition(DDA)[12]やData Independent Acquisition(DIA)[13]が標準化されてきた質量分析手法の系譜を継ぐ進歩であり、各種マススペクトルの同時計測を行う「次世代質量分析イメージング」への道を切り開くものです。また、本手法は特殊なマトリックス化合物を必要としないため、多くの現場で実施可能な汎用性(はんようせい)も備えています。
現在の生命科学は、遺伝子・タンパク質・代謝物のシングルセル(1細胞)解析と共に、各種の空間解析技術の研究開発が日進月歩で進んでいます。本研究で開発したSMASH imagingは、精度や深度の高い空間リピドミクス解析を可能にし、さらにトランスクリプトミクス(遺伝子発現の網羅的解析)やプロテオミクス(タンパク質の網羅的解析)との空間的な統合解析から「リピドームアトラス」の構築が進み、生命科学および医学研究の発展に大きく貢献することが期待されます。
補足説明
- 1.質量分析イメージング(MSI)
各種のイオン化法を用いて、組織切片などの2次元試料を格子状に計測(マッピング)することで、各ピクセルのマススペクトル(分子の質量情報)と空間情報(座標)を同時に取得する計測技術。UVレーザーを用いたMALDI([5]参照)以外にも、エレクトロスプレーによるDESI(Desorption ElectroSpray Ionization)やイオンビームによるSIMS(Secondary Ion Mass Spectrometry)などのMSI手法が存在する。MSIはMass Spectrometry Imagingの略。 - 2.イオンモビリティー
対向ガス(窒素やヘリウムなど)が充満した空間に電場をかけてイオンを通過させ、その速度を計測する手法。同じ質量を持つイオン同士であっても、イオンモビリティーでの速度(移動度)を計測することで、その立体的特性(大きさや形状、電荷を持つ構造部位の違いなど)を識別することができる。質量分析イメージングでは、検出分子を質量以外で分離・識別することができないため、LC-MS/MS([8]参照)と比べると同質量のイオン同士の構造識別が難しかった。しかし、近年ではこのイオンモビリティーを質量分析装置内に搭載した装置が多く登場し、質量分析イメージングでも使用されつつある。 - 3.タンデム質量分析
質量分析(Mass Spectrometry: MS)は、分子や原子を各種のイオン化法でイオン化し、検出することで分析物の質量を計測する分析法。タンデム質量分析(MS/MS)では、2段階の質量分析を行う。1回目はイオン化された全分子の質量を計測し、2回目は詳細な構造情報を取得するためにイオンにエネルギーや反応を加え、生じた断片化イオンを計測する。 - 4.MS/MSスペクトル
タンデム質量分析によって得られるマススペクトル。MS/MSスペクトルには、分析対象となった分子の部分構造の情報(断片化イオン)が含まれ、解析することで分子の詳細な構造決定ができる。 - 5.マトリックス支援レーザー脱離イオン化法(MALDI)
サンプル上に形成されたマトリックス結晶([6]参照)に対してUV(紫外線)レーザー(337ナノメートル(nm、1nmは10億分の1メートル)や355nm)照射によりエネルギーを加えることで、結晶中の分子の脱離とマトリックス化合物によるイオン化を促進するイオン化法。MALDIはMatrix Assisted Laser Desorption/Ionizationの略。 - 6.マトリックス結晶
MALDI質量分析においてサンプル(タンパク質や代謝物など)をイオン化するために混合する有機化合物(マトリックス化合物)の結晶。イオン化を支援(促進)するマトリックス化合物をメタノールやアセトニトリルなどの有機溶媒に溶かし、その溶液をサンプルに滴下したり塗布したりする。そうすると、有機溶媒によってサンプル中の分子が抽出され、溶液に含まれるマトリックス化合物と共に結晶を形成する。検体由来の分子とイオン化を促進するマトリックス化合物が共に含まれるこの結晶にUVレーザーを照射することでMALDIが実施できる。 - 7.レーザーマイクロダイセクション
レーザーマイクロダイセクション(Laser Microdissection)は、顕微鏡で観察しながらUVレーザーを使って組織切片の特定の領域や細胞だけを切り取って回収する技術。これにより、人間の目視レベルでは識別できない局所的な組織部位や細胞集団のみを回収して、脂質や代謝物のみならず遺伝子やタンパク質などを詳しく解析できる。 - 8.液体クロマトグラフィータンデム質量分析(LC-MS/MS)
液体クロマトグラフィーとタンデム質量分析を組み合わせた分析手法。まず、液体クロマトグラフィーで計測分子の物性の違いに応じて分子を分離し、次いで質量分析装置へと導入する。質量分析装置では、分子がイオン化され、イオン全体の質量と、イオンを断片化した部分構造の質量を計測する。バルクの計測手法(検体を破砕するなどして全体から抽出した分子を計測する手法。感度や検出範囲に優れる一方で空間情報は基本的に得られない)として今日のリピドミクスやメタボロミクスにおいて標準的な計測技術の一つ。 - 9.側鎖異性体
脂質の側鎖異性体とは、極性基や基本骨格などの基本的な構造や分子量は同じでありながら、分子内にある複数のアシル基(脂肪酸由来の側鎖)の組み合わせが異なる構造同士のこと。例えば、パルミチン酸(炭素数16・不飽和度0)とアラキドン酸(炭素数20・不飽和度4)の側鎖を持つ場合とリノール酸(炭素数18・不飽和度2)を二つ持つ場合が該当する(2本の側鎖を合算すると炭素数36・不飽和度4で分子量が一致する)。分子構造は似ているが、生体内での生合成経路や機能が異なる場合があり、近年の質量分析技術の向上によりその違いを識別して解析する研究が進んでいる。 - 10.UMAP
オミクスデータなど高次元データが持つ内在的な近傍構造(サンプル間の類似性)をできるだけ保持するよう最適化し、その違いを人間が判断しやすい2次元などの低次元空間へと写像する次元削減手法の一つ。UMAPはUniform Manifold Approximation and Projectionの略。 - 11.プリカーサーイオンとそのフラグメントイオン
プリカーサーイオンとは、質量分析において分子がイオン化された後、さらにMS/MS解析させる前の元となるイオンのこと。このプリカーサーイオンへエネルギーや反応を加え、構造が解離して生じるイオンをフラグメントイオン(断片化イオン)と呼ぶ。 - 12.Data dependent acquisition(DDA)
タンデム質量分析において、イオン強度値が多い数個~数十個のイオンに絞ってMS/MSスペクトルを取得する手法。 - 13.Data independent acquisition(DIA)
タンデム質量分析において、全体の質量範囲を数ダルトン(Da、1Daは12C原子の質量の12分の1)から数十Da幅に区切った各ウインドウについて走査的にMS/MSスペクトルを取得することで、実質的に検出イオンの全MS/MSスペクトルを取得する手法。得られるMS/MSスペクトルは複数イオンの混合マススペクトルとなるため、スペクトルのデコンボリューション(単一イオンに対応するマススペクトル抽出)や高度なデータ解析を要する。
研究チーム
理化学研究所 生命医科学研究センター メタボローム研究チーム
特別研究員 内野 春希(ウチノ・ハルキ)
客員研究員 津川 裕司(ツガワ・ヒロシ)
(東京農工大学 大学院工学研究院 教授)
チームディレクター 有田 誠(アリタ・マコト)
(慶應義塾大学 薬学部・薬学研究科 教授)
研究支援
本研究は、科学技術振興機構(JST)戦略的創造推進事業ERATO「有田リピドームアトラスプロジェクト(研究代表者:有田誠、JPMJER2101)」、ライフサイエンスデータベース統合推進事業統合化推進プログラム「次世代低分子マススペクトルデータベース シン・マスバンクの構築(研究代表者:松田史生、JPMJND2305)」、日本医療研究開発機構(AMED)ムーンショット型研究開発事業(JP22zf0127007)の助成を受けました。
原論文情報
- Haruki Uchino, Hiroshi Tsugawa, Makoto Arita, "SMASH Imaging: A Serial Matrix-Assisted Laser Desorption/Ionization Mass Spectrometry Strategy for High-Resolution Imaging Facilitates Dual-Polarity and MS2 Spatial Lipidomics on a Single Tissue Section", Analytical Chemistry, 10.1021/acs.analchem.5c03738
発表者
理化学研究所
生命医科学研究センター メタボローム研究チーム
特別研究員 内野 春希(ウチノ・ハルキ)
客員研究員 津川 裕司(ツガワ・ヒロシ)
チームディレクター 有田 誠(アリタ・マコト)
(慶應義塾大学 薬学部・薬学研究科 教授)
 内野 春希
内野 春希
 津川 裕司
津川 裕司
 有田 誠
有田 誠
JST事業に関すること
科学技術振興機構 研究プロジェクト推進部 ICT/ライフイノベーショングループ
今林 文枝(イマバヤシ・フミエ)
Tel: 03-3512-3528
Email: eratowww@jst.go.jp
報道担当
理化学研究所 広報部 報道担当
お問い合わせフォーム
慶應義塾 広報室
Tel: 03-5427-1541
Email: m-pr@adst.keio.ac.jp
科学技術振興機構 広報課
Tel: 03-5214-8404 / Fax: 03-5214-8432
Email: jstkoho@jst.go.jp
