理化学研究所(理研)生命機能科学研究センター 染色体分配研究チームの会沢 栄志 研究員(研究当時)、島本 走 基礎科学特別研究員、北島 智也 チームディレクターらの研究グループは、哺乳類の卵母細胞[1](卵子[1]の前駆細胞)が形成される一連の過程をライブイメージング[2]で連続観察することに成功しました。
本研究成果は、哺乳類の卵母細胞形成に関する定説の再検討を提起し、生殖補助医療に用いられる卵子の質の予測や制御に向けた新たな知見をもたらすと期待されます。
女性の生殖能力が確立されるためには、生殖細胞[3]である卵母細胞の形成が必須です。哺乳類では、卵母細胞の形成過程は胎児内で進行するため直接観察することはできず、その実態は謎に包まれてきました。
今回、研究グループは、マウス胎仔の生殖腺[3]を長期間にわたって体外培養しながら光学顕微鏡でライブイメージングする技術を開発し、卵母細胞の形成過程を動画で撮影することに成功しました。この動画から、将来卵母細胞となる細胞では細胞膜の突出や退縮(萎縮または消失する現象)が頻繁に起きていることを発見しました。また、非哺乳類動物に見られるように卵母細胞の形成には細胞小器官(オルガネラ)[4]を含む細胞質の細胞間移動を伴うと広く考えられてきましたが、マウスの卵母細胞形成ではそのような細胞間移動は見られませんでした。これらの結果は、哺乳類の卵母細胞の形成過程では、非哺乳類動物とは別の仕組みが働いている可能性を示唆しています。
本研究は、科学雑誌『EMBO Journal』オンライン版(4月21日付:日本時間4月21日)に掲載されました。
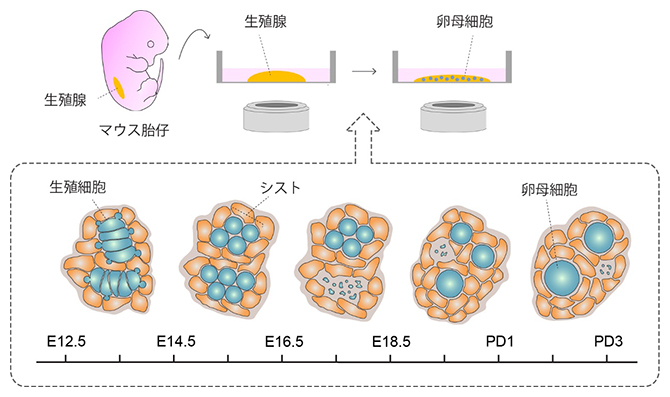
卵母細胞形成過程のライブイメージングが捉えた未知の生殖細胞動態
背景
生殖は、親から子へと遺伝情報が受け継がれる生命の根幹的なプロセスです。その情報の運び手となるのが生殖細胞です。女性の生殖細胞である卵母細胞は、成熟して卵子となり、精子と受精して次世代の出発点となります。また卵母細胞は、遺伝情報だけではなく初期発生に必要な細胞質成分や細胞小器官(オルガネラ)を受精卵に渡す役割も担います。従って、卵母細胞が正しく形成されることは、母から子への遺伝情報の継承と正常な胚発生に必須です。
卵母細胞が成体でも形成される昆虫や卵生の脊椎動物とは異なり、ヒトを含む哺乳類における卵母細胞の形成は胎児の中でのみ起こります。まず、生殖細胞が細胞分裂(体細胞分裂)を繰り返して、細胞同士がつながった「シスト[5]」と呼ばれる細胞集合体(生殖細胞シスト[5])ができます。次に、たくさんの生殖細胞のうち一部のみが卵母細胞として残り、他の細胞は消失します。残された卵母細胞はその後減数分裂[6]を開始しますが、原始卵胞[7]に包まれて細胞周期を停止します。この停止期間は、出生後の成長を経て性成熟し、卵子を排卵するために細胞周期を再開させるまで維持されます。ヒトではその期間は思春期以後から数十年に及び、この長い停止が保たれることが生殖能力の維持に重要です。つまり、胎児期における卵母細胞の形成は、出生後の生殖寿命を支える基盤を確立します。
卵母細胞の形成の仕組みは、これまでさまざまな動物で研究されてきました。例えば昆虫のハエでは、細胞シスト内でオルガネラを含む細胞質が細胞間を移動し、その移動先の細胞が卵母細胞となることが知られています。哺乳類でもこれとよく似たシスト構造が見られるため、生殖細胞シスト内の細胞間を細胞質およびオルガネラが移動することで卵母細胞が形成されるという仮説が広く受け入れられてきました。
しかし、哺乳類において生殖細胞シスト内で細胞質およびオルガネラの細胞間移動が本当に起きているのかは、これまで直接検証されていませんでした。さまざまな発達段階の生殖細胞を固定した標本観察からは、細胞質やオルガネラの移動を示すと考えて矛盾しない画像が得られていたものの、それだけでは実際に細胞質やオルガネラが細胞間を移動している証拠にはなりません。哺乳類の卵母細胞形成は胎児の中で進行するため、生きたままリアルタイムで動画に収めることで仮説を検証することは技術的に困難でした。
研究手法と成果
研究グループは、マウスをモデルに、哺乳類の卵母細胞の形成過程をリアルタイムで観察するライブイメージング技術の開発に取り組みました。まず、雌マウス胎仔から生殖腺を切り出し、それをガラス底面の培養皿で長期間培養して卵母細胞を形成させる技術を開発しました(図1A)。この体外培養では、生体内で卵母細胞形成の時期に特異的に見られる、相同染色体間の対合(たいごう)[6]や特徴的な遺伝子発現パターンなどが再現されていました。また、体外培養を約1カ月間にわたって継続したところ、生体内で成長した卵母細胞と同様のサイズの卵母細胞が得られました(図1B)。これらの結果から、今回開発した体外培養は、生体内における卵母細胞の形成をほぼ忠実に再現すると考えられました。
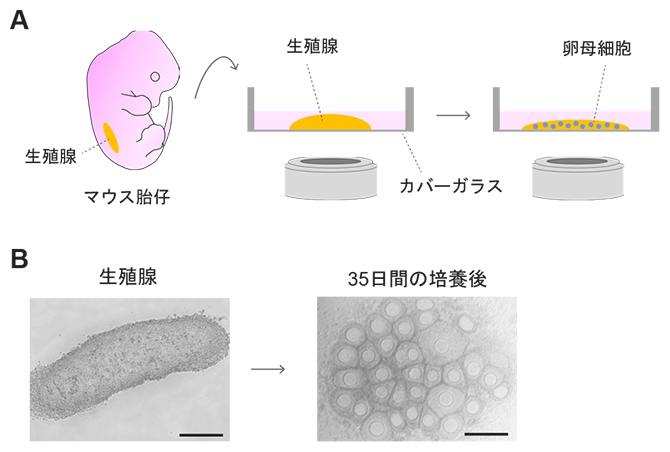
図1 マウス生殖腺の体外培養による卵母細胞形成
- A)マウス胎仔由来の生殖腺をガラス底培養皿上で体外培養し、顕微鏡下で観察する実験系の概略。
- B)生殖腺を35日間体外培養することで、卵母細胞を含む卵胞が形成される様子。スケールバーは200マイクロメートル(μm、1μmは100万分の1メートル)。
この体外培養を顕微鏡下で行うことで、卵母細胞の形成過程のライブイメージングが可能となりました。研究グループはまず、細胞膜を蛍光標識[2]するプローブを用いて、生殖細胞シストが見られる時期の細胞動態を動画撮影しました。その動画には、後に卵母細胞として残る生殖細胞が、時間進行に伴って細胞質の体積を増加させる様子が映し出されていました。重要なことに、その増加速度は、生殖細胞シストと考えられる細胞集団から分離した後に加速していました(図2A)。さらに動画では、生殖細胞シストと考えられる細胞集団を構成する生殖細胞が、一斉に消失する様子を捉えていました(図2B)。これらの観察は、生殖細胞シスト内で、細胞質が移動する先の生殖細胞が卵母細胞となるという従来仮説よりも、むしろ卵母細胞として後に残る生殖細胞が自律的に自身の細胞質を増加させるという新しい仕組みの存在を示唆しています。
この動画にはナレーションはありません
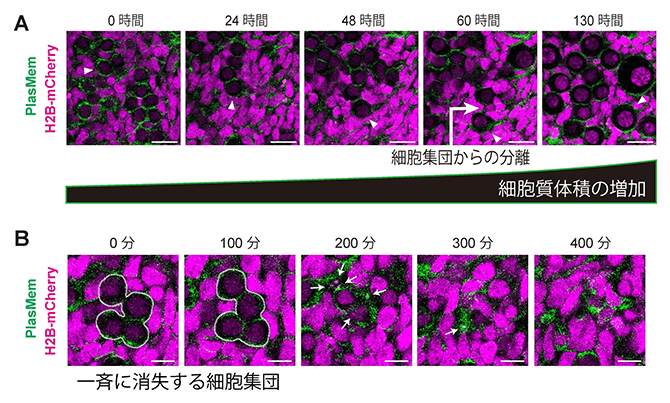
図2 生殖細胞シストから分離した卵母細胞の自律的な細胞質サイズ増大
- A)130時間のライブイメージングにより、卵母細胞が時間とともに細胞質体積を増加させる様子を示す。PlasMemは細胞膜を蛍光標識するプローブ。マゼンタ(H2B-mCherry)は細胞核。矢頭は同一の生殖細胞を示し、細胞集団から分離した後から細胞質体積の増加が加速している。
- B)生殖細胞シストを形成する細胞が同期的に消失する様子を示す(白色の点線で囲まれた細胞集団)。矢印は消失する生殖細胞を示す。
スケールバーはいずれも20μm。
また、生殖細胞の形成過程では、体細胞分裂から減数分裂への切り替えが重要な転換点となります。しかしこのタイミングで細胞の振る舞いにどのような変化が生じているかはよく分かっていません。そこで、生殖細胞に特徴的な細胞動態がないかを探索したところ、生殖細胞が体細胞分裂の繰り返しを完了する時期に限って、一過的な細胞膜の突出(細胞膜ブレビング[8])が頻繁に見られることが分かりました。この細胞膜ブレビングは、生殖細胞の細胞膜が周縁の体細胞に向かって球状に膨らんで消えるという特徴を持っていました(図3)。また、減数分裂との関連を調べたところ、この細胞膜ブレビングは、生殖細胞の減数分裂開始を誘導する細胞シグナル伝達経路を介して活性化することが明らかになりました。
生殖細胞で活発な細胞膜ブレビングが起きていることはこれまで知られておらず、今回開発した卵母細胞のライブイメージング技術が、卵母細胞形成に伴う未知の細胞動態を発見するために有用であることを示しています。
この動画にはナレーションはありません
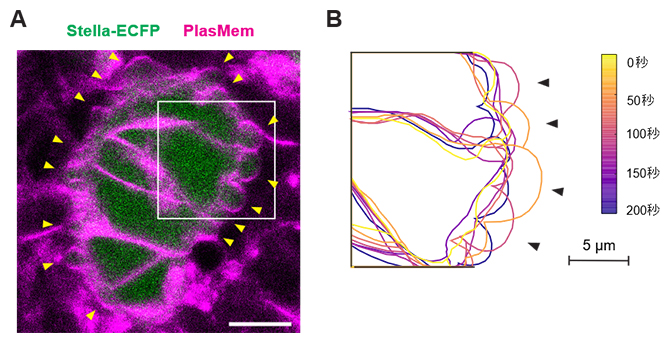
図3 生殖細胞で観察された時期特異的に活発化する細胞膜ブレビング
- A)生殖細胞(生殖細胞特異的タンパク質Stellaとシアン蛍光タンパク質ECFPの融合タンパク質Stella-ECFPでマーク)が活発な細胞膜ブレビング(矢頭)を示す様子。PlasMem(マゼンタ)は細胞膜プローブ。白枠はB)で拡大して示した領域。スケールバーは10μm。
- B)細胞膜ブレビングに伴う細胞膜の形態変化を、時系列に応じて色分けして示したもの。
研究グループは続いて、生殖細胞シスト内の細胞間でオルガネラの移動が起きているのかを検証しました。従来の仮説では、細胞間で移動するオルガネラとしてミトコンドリア[9]と中心体[10]が挙げられています。そこで、顕微鏡下で選択的に光照射することで、特定の細胞のミトコンドリアおよび中心体を蛍光標識できる実験系を構築しました。シスト内にある複数の生殖細胞のうち、一つのみの生殖細胞についてミトコンドリアを蛍光標識したところ、標識されたミトコンドリアはその細胞内に留まり続け、隣り合う生殖細胞に移動することはありませんでした(図4)。同様に、中心体を標識しても、細胞間の移動は見られませんでした。この観察は、哺乳類における卵母細胞の形成はシスト内の細胞間オルガネラ移動を伴う、という従来仮説とは異なる仕組みが存在することを示唆しています。
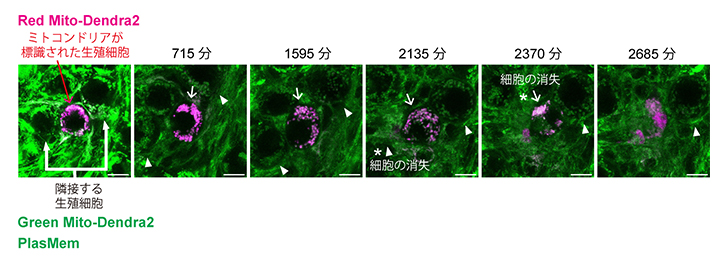
図4 生殖細胞シスト内で細胞間を移動しないオルガネラ
生殖細胞の細胞膜をPlasMem(緑)で、生殖細胞内のミトコンドリアをGreen Mito-Dendra2(緑)で標識し、光照射により特定の生殖細胞(矢印)内のミトコンドリアのみをRed Mito-Dendra2(紫色)に転換して追跡した。ミトコンドリアは、紫色標識から2,370分後に細胞が消失しても、その前後を含めて隣接細胞(矢頭)へ移動しないことが確認された。
今後の期待
本研究の成果から、哺乳類における卵母細胞の形成には未知の機構が潜んでいることが示唆されました。これまで、胎児の中で起こる卵母細胞の形成を観察することはできず、その理解は非哺乳類モデルから得られた知見に基づき推測することしかできませんでした。しかしヒトを含む哺乳類では、卵母細胞形成が胎児期のみに限られ、出生時の卵子の数がその後の生殖寿命全体にわたる基盤を確立するという特徴があります。哺乳類に特異的な卵母細胞の形成機構は、哺乳類を用いた研究でしか理解することができません。本研究によって確立されたライブイメージング技術により、マウス卵母細胞の形成過程を観察することが可能となりました。これにより、ヒトを含む哺乳類における卵母細胞形成機構の理解に向けた新たな研究の展開が期待されます。
少子高齢化社会において、女性のリプロダクティブ・ヘルス[11]は最重要課題の一つです。胎児期に形成された卵母細胞は後に卵子となり次世代の出発点となることから、卵子の質は不妊治療や生殖補助医療の成否に影響します。哺乳類における卵母細胞形成の機構を明らかにする研究は、卵子の質の予測や制御に向けた基盤知見を与えることが期待されます。
補足説明
- 1.卵母細胞、卵子
卵母細胞は受精能を持たない発達段階の生殖細胞([3]参照)であり、卵子は受精可能な生殖細胞である。卵母細胞は胎児期に形成され卵巣内に蓄積される。長期の停止期間を経た後、減数分裂を再開して成熟し、卵子となる。 - 2.ライブイメージング、蛍光標識
ライブイメージングは、生きた細胞や組織をそのままの状態で観察し、時間経過に伴う動態を連続的に記録する手法である。固定標本では捉えられない細胞の動きや変化を可視化できる。蛍光標識は、ライブイメージングで特定の細胞やタンパク質を追跡する手法の一つで、細胞毒性の低い低分子蛍光色素などが用いられる。 - 3.生殖細胞、生殖腺
生殖細胞は、次世代へ遺伝情報を伝える役割を持つ細胞であり、精子や卵子のもととなる細胞である。体細胞とは異なり、減数分裂を行うことで染色体数を半減させ、受精により元の染色体数を回復させる。生殖腺は、生殖細胞を含む器官であり、発生の進行に伴い雌では卵巣、雄では精巣へと分化する。胎児内に未分化な状態で存在し、生殖細胞が集積して増殖や分化を進める場となる。 - 4.細胞小器官(オルガネラ)
細胞の中で一定の形態や機能を持つ構造体の総称。ミトコンドリアや液胞など脂質膜を持つものと、中心体のように膜を持たない非膜型細胞小器官がある。 - 5.シスト、生殖細胞シスト
シスト(cyst)は、生物体に見られる袋状の構造の総称。生殖細胞シストとは、分裂した生殖細胞が完全には分離せず、細胞間が連結したまま集合体を形成した構造である。この構造は多くの動物種で見られ、細胞間で物質や情報を共有する場として機能すると考えられている。 - 6.減数分裂、対合(たいごう)
減数分裂は、生殖細胞に特有の細胞分裂様式であり、2回の連続した分裂によって染色体数を半減させる。1回目の分裂(減数第一分裂)で相同染色体が互いに接着(対合)し、相同染色体が分配される。続く2回目の分裂(減数第二分裂)で姉妹染色分体が分配されることで配偶子(精子や卵子)が形成され、受精後に正常な染色体数が回復される。 - 7.原始卵胞
卵母細胞と、卵母細胞を取り巻く体細胞から成る構造を卵胞と呼ぶ。原始卵胞は休眠状態の卵胞を指し、活性化すると発育卵胞(一次卵胞、二次卵胞)へと変化する。活性化後は休眠状態に戻ることはできず、卵子となるか、発育途中で閉鎖する運命にある。 - 8.細胞膜ブレビング
ブレビング(blebbing)とは、細胞膜が局所的に球状に膨らみ、突出と収縮を繰り返す現象である。細胞の移動や形態変化、細胞内圧の変化などに関連して生じることが知られている。 - 9.ミトコンドリア
ミトコンドリアは、細胞内に存在する細胞小器官(オルガネラ)の一つであり、エネルギー産生を担う。独自のDNAを持ち、細胞の代謝や生存に重要な役割を果たす。 - 10.中心体
中心体は、細胞分裂時に紡錘体を形成する中心となる細胞内構造である。微小管の形成を制御し、染色体の正確な分配に重要な役割を担う。多くの動物細胞に存在する。 - 11.リプロダクティブ・ヘルス
性と生殖に関する健康。世界保健機関(WHO)では、「生殖に関するあらゆる状況について、単に疾病や障害がないというだけでなく、肉体的、精神的、社会的に完全に良好な状態であること」と定義されている。詳しくはWHOのサイト(英語)参照。
研究グループ
理化学研究所 生命機能科学研究センター
染色体分配研究チーム
研究員(研究当時)会沢 栄志(アイザワ・エイシ)
(ハーバード大学(米国)研究員)
基礎科学特別研究員 島本 走(シマモト・ソウ)
チームディレクター 北島 智也(キタジマ・トモヤ)
(生命機能科学研究センター 副センター長)
配偶子形成研究チーム
テクニカルスタッフⅠ 梶川 絵理子(カジカワ・エリコ)
チームディレクター 澁谷 大輝(シブヤ・ヒロキ)
生体モデル開発チーム
テクニカルスタッフⅠ 原 淳子(ハラ・ジュンコ)
技師 阿部 高也(アベ・タカヤ)
研究支援
本研究は、理化学研究所運営費交付金(生命機能科学研究、理研新領域開拓課題「長時間分子生物学(領域代表者:北島智也)」)で実施し、日本学術振興会(JSPS)科学研究費助成事業学術変革領域研究(A)「動的な生殖ライフスパン:変動する生殖細胞の機能と次世代へのリスク(領域代表者:北島智也)」、同基盤研究(A)「人工動原体の構築による染色体分配の機構の解明(研究代表者:北島智也)」、同基盤研究(B)「哺乳類卵母細胞における紡錘体二極化の機構の解明(研究代表者:北島智也)」、内藤記念特定研究助成金「卵母細胞における染色体分配エラーの時空間経路の解明」による助成を受けて行われました。
また、会沢栄志は、JSPS海外特別研究員制度(202460115)の支援を受け、研究を遂行しました。
原論文情報
- Eishi Aizawa, So Shimamoto, Eriko Kajikawa, Junko Hara, Takaya Abe, Hiroki Shibuya and Tomoya S. Kitajima, "Dynamic blebbing and absence of organelle transfer during mouse oocyte formation", EMBO Journal, 10.1038/s44318-026-00780-6
発表者
理化学研究所
生命機能科学研究センター 染色体分配研究チーム
研究員(研究当時)会沢 栄志(アイザワ・エイシ)
基礎科学特別研究員 島本 走(シマモト・ソウ)
チームディレクター 北島 智也(キタジマ・トモヤ)
報道担当
理化学研究所 広報部 報道担当
お問い合わせフォーム
