理化学研究所(理研)生命機能科学研究センター 発生ゲノムシステム研究チームの近藤 武史 チームディレクター、水野 苑子 リサーチアソシエイトらの共同研究チームは、動物の発生過程において、細胞が発現するマイクロペプチド[1]がタイマーのように機能し、特定のタイプへの細胞運命[2]の誘導が可能な"限られた時間"を規定することを発見しました。
本研究成果は、精巧な機能と形を持ち合わせる動物の器官が、発生という時間の流れの中で、段階的に仕組みを切り替えながらどのように形作られていくのかという理解を深めるとともに、医学や生物工学など幅広い科学分野で、生命現象の時間軸に関する知見を必要とする研究開発へ貢献することが期待されます。
細胞分化[2]は、いくつもの制御メカニズムが切り替わりながら進行します。ショウジョウバエ[3]の呼吸器である気管では、まず特定の細胞集団に気管への細胞運命が誘導され、その後の形態形成を経て、正しい場所にある細胞のみがその運命を維持し、気管細胞へと分化します。しかし、この細胞運命の制御メカニズムの切り替えを可能にする仕組みは、これまでほとんど分かっていませんでした。
共同研究チームは、気管への細胞運命の誘導開始に、11もしくは32アミノ酸長から成るマイクロペプチドが重要な役割を果たしていることを発見しました。さらにこのマイクロペプチド遺伝子の発現が一過的であり、その発現終了が、気管への細胞運命を「誘導する段階」から「維持する段階」へと切り替える合図として機能する、いわば「タイマー」の役割を果たしていることを明らかにしました。
本研究は、科学雑誌『Proceedings of the National Academy of Sciences of the United States of America(PNAS)』オンライン版に3月2日の週に掲載されます。
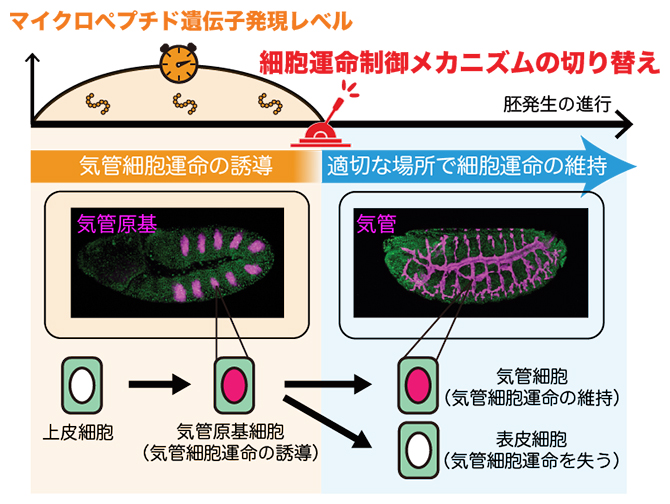
マイクロペプチドタイマーによる細胞運命制御メカニズムの切り替え
背景
私たちの体を構成する多様な細胞は、元は一つの受精卵が分裂を繰り返しながら増殖し、特定の機能を発揮する細胞タイプへと分化してきたものです。従って、この細胞分化の過程において一つ一つの細胞の運命がどのように決定していくのかは、生物の発生の仕組みを理解する上で不可欠な問いです。
細胞運命は、他の細胞からの分泌因子など外部からのさまざまな分子シグナルによって制御されます。その分子シグナルの種類やレベルなどの情報を基に、細胞は組織内での位置を読み取りながら、最終的に細胞運命を決定していきます。これらの細胞外からの情報は細胞内の転写因子[4]を介して遺伝子発現の変化として統合され、細胞運命の決定へとつながります。一方で発生過程では、個々の細胞運命の決定と並行して、組織の形づくり(形態形成)も進行します。近年では、組織の形の変化に起因する圧力や張力などの物理的な刺激[5]も細胞運命に影響を与え、各細胞タイプが組織内で適切に配置されるために重要であることが明らかになってきました。しかしながら、分子シグナルによる化学的な制御と、力学的刺激などの物理的な制御という二つの異なる仕組みを、細胞がどのように順序立てて用い、細胞運命の決定を進めているのかはよく分かっていませんでした。
研究手法と成果
共同研究チームは、ショウジョウバエの呼吸器である気管の発生をモデルとして研究しました。気管の発生は、受精から約4時間経過した胚の表面を覆う上皮細胞[6]シート内の、それぞれ約60細胞から成る左右10対の領域において始まります。各領域は気管原基と呼ばれ、マスター制御因子[7]をコードする遺伝子として知られるtrachealess(trh)の発現が誘導されることで気管への細胞運命が開始され、管状の組織構造から成る気管の形成を進めます(図1)。trhの発現は、周辺細胞が分泌する分子シグナルによって活性化されるJAK-STAT経路[8]により誘導されることが知られています。さらに近藤チームディレクターらはこれまでに、trhを発現した気管原基細胞の全てが胚の内部に入り込んで気管を構築するのではなく、一部は胚の表面にとどまること、そして表面に残った細胞ではtrh発現が失われ、最終的には気管ではなく表皮細胞へと分化することを明らかにしています注1)(図1)。このことは、気管細胞の分化が、「気管細胞運命の誘導開始」とその後の「内部へ陥入し気管構造を構築する細胞のみでの気管細胞運命の維持」という2段階の制御により進むことを示唆しています。しかしながら、細胞運命の開始と維持という異なる制御メカニズム間で、どのように切り替えが起こるのかは不明でした。
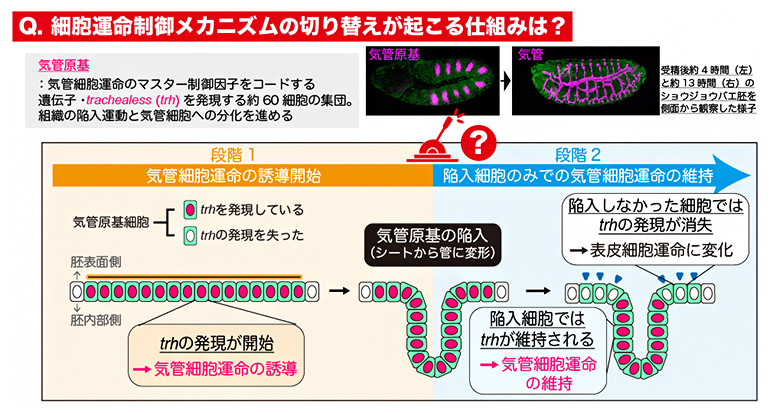
図1 気管細胞運命の2段階制御システム
ショウジョウバエの気管の発生は、胸部から腹部体節にかけて左右10対の領域で始まり、それぞれの領域で上皮細胞シート内の約60細胞がtrhを発現することで気管へと分化する細胞運命(気管細胞運命)が誘導される(気管原基細胞)。その後、気管原基は胚内部に陥入して管状の構造をつくる。そして、陥入した細胞はtrhを発現し続けて気管運命を維持する一方で、陥入しなかった細胞はtrhを発現しなくなり、気管ではなく表皮へと分化する細胞運命(表皮細胞運命)へと変化する。この「開始」と「維持」という二つの異なる細胞運命制御メカニズムの間で切り替えが起こる仕組みは不明だった。
今回、共同研究チームは、気管への細胞運命の誘導が開始される時期特異的に、polished rice(pri)遺伝子が発現することに着目しました。priから転写されたmRNAは四つの機能的なオープンリーディングフレーム(ORF)[1]を持ち、それぞれ11もしくは32アミノ酸長のマイクロペプチド(Priペプチド)をコードします(図2A)。
初めに、Priペプチドが気管への細胞運命の誘導に関与する可能性を検証しました。priの気管原基における発現タイミングを多重in-situハイブリダイゼーション法[9]により詳細に解析したところ、priはtrh発現開始よりも先に一過的に発現し、気管原基の陥入が始まる頃には発現がなくなることが明らかとなりました(図2B)。さらに、priを欠損させた胚の気管原基を解析すると、正常胚と比較してtrh発現細胞数が減少しており(図2C)、陥入する細胞数も減少していました。また、既知のtrh発現誘導因子であるJAK-STATシグナルを阻害した胚では、priは依然として一過的な発現を示し、同じ領域でtrh発現が見られましたが、このtrh発現はpri同様に一過的で、持続することなく消えてしまいました。さらに、JAK-STATシグナルとpri発現の両方を阻害すると、trhの発現が全く誘導されず気管が形成されませんでした。
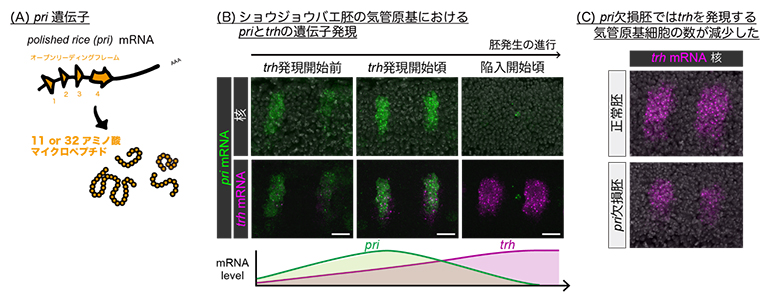
図2 気管原基領域に一過的に発現するpri遺伝子と気管細胞運命の開始
- (A)pri遺伝子の模式図。polished rice(pri)遺伝子座から転写されたmRNAは四つのオープンリーディングフレーム(ORF)を持ち、それぞれから11もしくは32アミノ酸長のマイクロペプチド(Priペプチド)が翻訳される。
- (B)気管原基におけるpriとtrhの発現パターンの比較。pri(緑)はtrh(マゼンタ)に先立って発現が始まり、その後trhがpriと重なるように発現し始める。気管原基が陥入し始める頃、priの発現は消失しtrh発現のみが残る。核(白)は全ての細胞の核を染めるDAPIのシグナル。写真の下は、それぞれのmRNA量の時間変化を比較したグラフ。スケールバーは20マイクロメートル(μm、1μmは100万分の1メートル)。
- (C)priを欠損させた胚の気管原基を解析すると、正常胚と比較してtrh発現細胞数が減少した。
これらの結果から、priは予定気管原基領域に一過的に発現することで適切な細胞運命の誘導開始に重要な役割を果たす一方で、JAK-STATシグナルは特にその誘導の増強に関わっており、この並行した制御の両方がそろうことで、適切な気管への細胞運命の誘導が実現していることが示唆されました。
次に、気管陥入後も活性化し続けるJAK-STATシグナルと対照的にpriの発現が一過的であることに着目し、その意義に迫るため、priの発現を人工的に延長させた胚の解析を行いました。その結果、陥入しなかった気管原基細胞で、本来は消失するはずのtrhが発現し続けてしまうことを発見しました(図3A)。従って、priは気管への細胞運命の開始に必要であると同時に、その速やかな消失が、細胞運命の開始メカニズムを終結させ、陥入した細胞のみで維持するメカニズムに切り替える鍵であると考えられました。
最後に共同研究チームは、priがtrh発現を誘導する分子メカニズムの解明を進めました。近藤チームディレクターらは先行研究で、Priペプチドは転写抑制因子Shavenbaby(抑制型Svb)の部分的分解を媒介し、下流遺伝子の転写を活性化する活性型Svbへと転換することを明らかにしていました注2)。解析の結果、気管への細胞運命の誘導においても、PriペプチドはSvbの活性転換を介してtrhの発現を制御しており、特に抑制型Svbの消失が重要であることが明らかになりました(図3B)。また、priの発現が消失した後に抑制型Svbが再び蓄積することが、胚表面に残った気管原基細胞におけるtrh発現の抑制に寄与していることも示されました。
興味深いことに、陥入した気管原基細胞は、抑制型Svbが蓄積してもtrh発現を維持し続けます。このことは、陥入した細胞は未知の仕組みによって抑制型Svbの作用を回避してtrh発現を持続していることを示唆しており、形態形成に依存した細胞運命の維持を制御する重要な鍵であると考えられます(図3B)。
管状構造という組織の形と同調して遺伝子発現を維持するメカニズムは大きな謎として残されていますが、今後、抑制型Svbの作用が組織形状によって異なる理由を解明することで、形態形成と細胞運命の維持をつなぐ原理の理解がさらに進むことが期待されます。
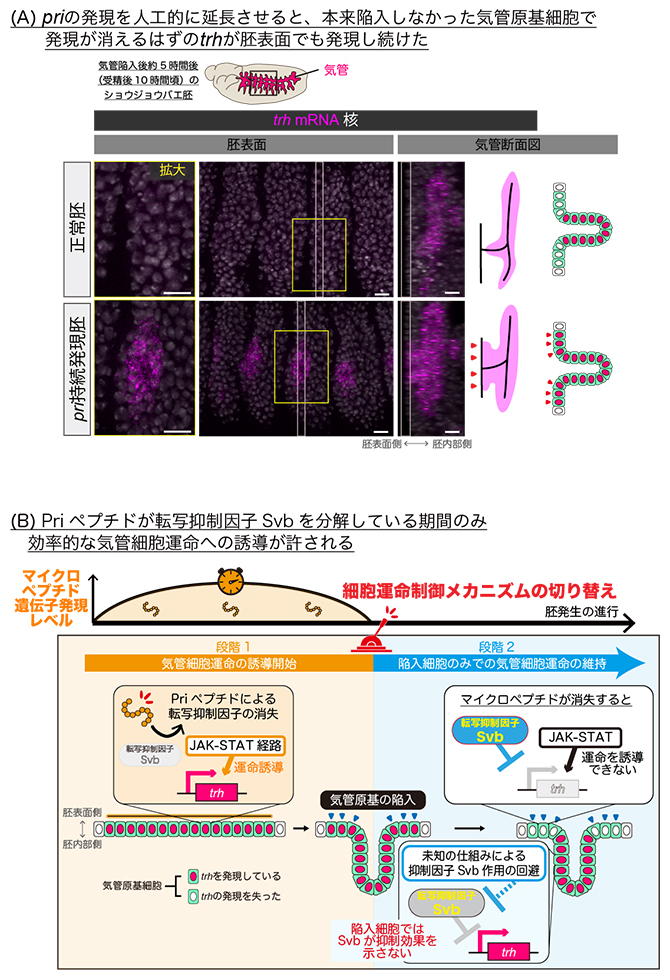
図3 気管細胞運命誘導の期間を決める一過的なpri遺伝子の発現
- (A)priの発現を人工的に延長させることで、priの一過的な発現パターンを乱す実験を行ったところ、陥入しなかった細胞で本来ならば発現が消えるtrhが、胚表面でも発現し続けた。胚イラスト内の四角形の枠は観察領域(中央の写真)を示す。黄線で囲った領域の胚表面の拡大図を左に、白線で囲んだ領域の断面図を右に示す。スケールバーは10μm。
- (B)一過的なpri発現が、気管細胞運命の誘導段階から維持段階へと切り替える仕組み。Priペプチドによりtrhの発現を抑制する転写抑制因子Svb (抑制型Svb)が消失すると、trh発現が開始し気管細胞運命が誘導され、さらに周辺細胞からの刺激を受けて活性化しているJAK-STAT経路の作用により気管細胞運命の誘導が増強される(段階1)。その後、pri発現がなくなると、非陥入細胞でJAK-STAT経路が活性化していても抑制型Svbが存在するためtrhの発現が抑制される(段階2)。陥入細胞でも抑制型Svbが蓄積しているが、未知の仕組みでtrhの発現が持続していると考えられる。
- 注1)2019年8月29日プレスリリース「動物の発生において形と機能を調和させる仕組みを発見」
- 注2)Kondo, T., Plaza, S., Zanet, J., Benrabah, E., Valenti, P., Hashimoto, Y., Kobayashi, S., Payre, F., and Kageyama, Y. (2010). Small Peptides Switch the Transcriptional Activity of Shavenbaby During Drosophila Embryogenesis. Science 329, 336-339.
今後の期待
近年、ヒト、ショウジョウバエ、酵母など幅広い真核生物のmRNAから、これまで見逃されてきた100アミノ酸以下の短いORFがマイクロペプチドとして翻訳されている例が明らかとなってきました。現在では数千を超えるマイクロペプチドが報告され、DNA修復や腫瘍形成など重要な生命現象への関与や、創薬の標的・モデルとなる可能性が注目されています。しかし、個々の詳細な機能解析は限られており、多様な生命現象におけるマイクロペプチドの影響は十分に解明されていません。
本研究は、11もしくは32アミノ酸のPriマイクロペプチドが細胞運命の誘導を可能にする"限られた時間"を定める機能を明らかにしました。小さなペプチドが重要な機能を担う例としてインスリンなどのホルモンやオキシトシンなどの神経ペプチドが知られていますが、これらは前駆体タンパク質から切断されて活性を持つペプチドが産生される点で、マイクロペプチドと異なります。
共同研究チームは、マイクロペプチド特有の合成や分解の速さが、精密な時間制御因子として適している可能性を考えています。生物の発生に限らず、概日リズムや薬剤耐性などあらゆる生命現象の理解において、時間軸の視点は不可欠です。従って本研究成果は、基礎生物学分野だけでなく創薬や発生工学を含む幅広い生命科学分野に貢献する知見であることが期待されます。
補足説明
- 1.マイクロペプチド、オープンリーディングフレーム(ORF)
DNAやmRNAの塩基配列を5'末端側から遺伝暗号表に基づいて読んでいくと、一つの開始コドンから次の終止コドンまで連続する塩基配列がしばしば登場する。この配列はタンパク質あるいはペプチドとして翻訳される可能性があり、オープンリーディングフレーム(open reading frame:ORF)と呼ばれる。マイクロペプチドはmRNA上の短いORFから翻訳されるペプチド。100アミノ酸以下のORFはランダムなDNA配列上にも確率的に高頻度で発生するため、実際に翻訳されているのか、また機能的なアミノ酸配列であるかを推定することが難しかった。近年では、翻訳されるORFを特定するリボソームプロファイリング法をはじめとした技術発展により、多様な真核生物で機能未知のマイクロペプチドの発現が数多く報告されている。 - 2.細胞運命、細胞分化
細胞分化とは、受精卵や幹細胞などのタイプが定まっていない細胞から、免疫細胞や筋細胞など特殊な機能を持った細胞になること。細胞運命とは、その細胞が将来どのタイプの細胞へと分化していくかという「方向性」のこと。細胞運命の決定過程とは、発生の過程で周囲のシグナルや環境による誘導に応答しながら、分化の方向性が段階的に絞り込まれていくプロセス。ただし、この運命は発生の途中で変わることもある。同じDNAを持つ細胞も、異なる細胞運命決定過程を経て、異なる遺伝子を発現することで、それぞれ異なる形や働きを持つ細胞へと分化する。 - 3.ショウジョウバエ
代表的なモデル生物。繁殖や飼育が容易で、染色体の少なさなど遺伝学的な解析に優れた特徴を持っている一方、ヒトと共通した器官や遺伝子を数多く持つ。 - 4.転写因子
DNAに結合して遺伝子発現を制御するタンパク質。 - 5.物理的な刺激
遺伝子発現の変化やシグナル伝達などの生化学的な変化とは対照的に、細胞が受ける力や、基質の硬さなどの物理要因が細胞に与える刺激のこと。組織の形態形成プロセスでは、その組織を構成する細胞や周囲の細胞が、押されたり、形が変わったりと、いろいろな物理的な刺激を受ける。また、組織の形状(Geometry)も一種の物理的な情報と捉えることができる。 - 6.上皮細胞
密着して並び、身体の表面や、消化管や呼吸器の表面など、外界との境界を覆う細胞。外界からのバリアや、物質交換の機能を有する。ショウジョウバエ初期胚の表面は1層の上皮細胞(上皮細胞シート)から成る。 - 7.マスター制御因子
細胞運命の決定に重要な役割を果たし、分化に必要な遺伝子群の発現を誘導する中心的な制御因子。ほとんどの場合は転写因子である。 - 8.JAK-STAT経路
細胞外の分子(サイトカインなど)を受け取った細胞膜表面の受容体が、細胞内の酵素JAKと転写因子STATを介して遺伝子発現を変化させるシグナル伝達経路。ヒトやショウジョウバエを含む広い生物種で保存されていて、免疫応答におけるサイトカインの作用機構として広く知られている。一方で、発生過程においても細胞の増殖や分化、運命決定を制御するなど重要な役割を果たしている。 - 9.in-situハイブリダイゼーション法
DNAやRNAが相補的な塩基対を形成する(ハイブリダイゼーションする)性質を用いて、目的の配列を有するRNAやDNAの組織内局在を可視化する手法。例えば、ショウジョウバエ胚が発現する特定のmRNA配列に相補的な配列を持つ1本鎖DNAを蛍光修飾し、ハイブリダイゼーションさせることで、蛍光顕微鏡によりmRNA発現の空間パターンを観察することができる。
共同研究チーム
理化学研究所 生命機能科学研究センター 発生ゲノムシステム研究チーム
チームディレクター 近藤 武史(コンドウ・タケフミ)
(京都大学 大学院生命科学研究科 客員准教授)
リサーチアソシエイト 水野 苑子(ミズノ・ソノコ)
(京都大学 大学院生命科学研究科 大学院生(研究当時))
京都大学 大学院生命科学研究科
教授(研究当時)上村 匡(ウエムラ・タダシ)
(現 京都大学 名誉教授)
研究支援
本研究は、理化学研究所運営費交付金(生命機能科学研究)で実施し、日本学術振興会(JSPS)科学研究費助成事業基盤研究(B)「上皮形態形成における組織形状と細胞分化の調和機構の解明(研究代表者:近藤武史、JP20H03258)」、同学術変革領域研究(A)「メカノ-ゲノムクロストークが制御する上皮組織の自律的秩序化(研究代表者:近藤武史、JP22H05167)」、同特別研究員奨励費「マイクロペプチドが上皮シート陥入を制御するメカニズムの解明(研究代表者:水野苑子、JP22J14899)」、科学技術振興機構(JST)創発的研究支援事業「器官構築を司る多階層情報フィードバックの解明(研究代表者:近藤武史、JPMJFR204V)」、同次世代研究者挑戦的研究プログラム(SPRING)「京都大学大学院教育支援機構SPRINGプログラム(JPMJSP2110)」による助成を受けて行われました。
原論文情報
- Sonoko Mizuno, Tadashi Uemura, Takefumi Kondo, "Pri Micropeptide Functions as a Cell-Intrinsic Timer Controlling the Transient Phase of Cell Fate Induction", Proceedings of the National Academy of Sciences of the United States of America(PNAS), 10.1073/pnas.2511138123
発表者
理化学研究所
生命機能科学研究センター 発生ゲノムシステム研究チーム
チームディレクター 近藤 武史(コンドウ・タケフミ)
リサーチアソシエイト 水野 苑子(ミズノ・ソノコ)
 水野 苑子
水野 苑子
 近藤 武史
近藤 武史
発表者のコメント
ゲノム―細胞―組織の階層を超えたフィードバックを理解する――。その研究指針に共鳴し、本研究室に飛び込みました。個々の細胞運命と組織レベルの秩序がどのように連関しているのか。その仕組みに迫れたこと、そして転写抑制因子の機能が組織の形によって異なるという新たな不思議が浮かび上がったことをうれしく思います。これからさらに、器官、個体、個体群……多様な階層を横断しながら生命現象を捉えていきたいです。(水野 苑子)
JST事業に関する問い合わせ
科学技術振興機構 創発的研究推進部
東出 学信(ヒガシデ・タカノブ)
Tel: 03-5214-7276
Email: souhatsu-inquiry@jst.go.jp
報道担当
理化学研究所 広報部 報道担当
お問い合わせフォーム
科学技術振興機構 広報課
Tel: 03-5214-8404
Email: jstkoho@jst.go.jp
