理化学研究所(理研)生命機能科学研究センター 神経幹細胞研究チームの福井 雅弘 リサーチ・アソシエイト、影山 龍一郎 チームディレクターらの国際共同研究グループは、神経幹細胞[1]を活性化する新たな手法により、アルツハイマー病[2]モデルマウスの病態を改善することに成功しました。
本研究成果は、アルツハイマー病などの神経変性疾患の新たな治療法の開発や、脳の老化メカニズムの解明に向けた基盤的研究に貢献すると期待されます。
記憶や学習、認知機能など脳の働きに重要な神経細胞は、神経幹細胞からつくられます。神経幹細胞は胎生期に活発に増殖し、大量の神経細胞をつくり出すことで脳が発達します。大人の脳にも神経幹細胞は存在しますが、老化に伴いその機能は低下し、神経新生[3]がほとんど起こらなくなります。
今回、国際共同研究グループは、神経幹細胞を活性化する手法iPaD[4](inducing Plagl2 and anti-Dyrk1a)を用いてアルツハイマー病モデルマウスを解析しました。その結果、神経新生が活性化されるとともに、脳内に蓄積する異常タンパク質(アミロイドβ[2])が減少し、認知機能が改善することを明らかにしました。さらに、iPaDによって発現が変化する下流遺伝子の中でも、Prkag2[5]を抑制することが特に強い効果を示すことを見いだしました。これらの成果は、神経新生の活性化がアルツハイマー病の病態改善につながる可能性を示すものです。
本研究は、科学雑誌『Cell Reports』(2026年4月28日号)の掲載に先立ちオンライン版(4月9日付)に掲載されました。
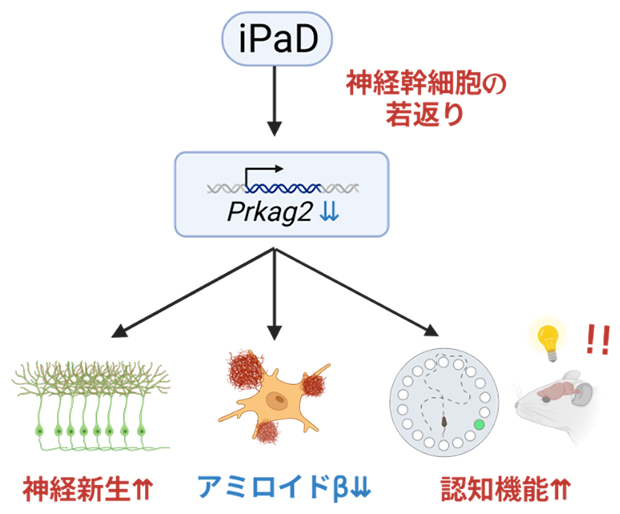
iPaDによる神経幹細胞の若返りとアルツハイマー病病態の改善
背景
私たちの脳は、胎児期の神経幹細胞が活発に増殖・分化して生み出された大量の神経細胞によってつくられます。出生後も、脳の一部では生涯にわたり新しい神経細胞が生まれる「神経新生」が起こっており、特に海馬[6]では、神経幹細胞が活性化されて新しい神経細胞がつくられ、学習や記憶に重要な役割を果たします。しかし、神経幹細胞の機能は加齢とともに低下し、神経新生の減少や認知機能の衰えの一因になると考えられています。
アルツハイマー病は代表的な認知症であり、脳内にアミロイドβと呼ばれる異常タンパク質が蓄積することで、神経細胞の障害や記憶障害が引き起こされます。この疾患では神経新生も低下していることが知られています。そのため、神経新生を活性化することで認知機能を改善できる可能性が期待されます。
しかしこれまでの研究では、神経新生を一時的に活性化しても、アミロイドβの蓄積を減らすことは難しく、根本的な治療にはつながらないという課題がありました。また、神経幹細胞を過剰に活性化すると、神経幹細胞が枯渇して神経新生自体が起きなくなってしまうことも分かっており注1)、持続的かつ安全に神経新生を活性化する方法の開発が求められていました。
- 注)Sueda, R., Imayoshi, I., Harima, Y., and Kageyama, R. (2019). High Hes1 expression and resultant Ascl1 suppression regulate quiescent vs. active neural stem cells in the adult mouse brain. Genes Dev. 33, 511-523.
研究手法と成果
国際共同研究グループは先行研究で、加齢によって機能が低下したマウスの神経幹細胞を「若い状態」に戻す新たな手法iPaD(inducing Plagl2 and anti-Dyrk1a)を報告しました注2)。iPaDは、胎仔期の脳に強く発現する遺伝子(Plagl2)を活性化し、同時に老化神経幹細胞で強く発現している遺伝子(Dyrk1a)を抑制するよう設計された手法です。これらの遺伝子操作をレンチウイルス[7]を用いて神経幹細胞に導入することで、神経幹細胞の機能を保ちながら神経新生を活性化することが可能になります。本研究では、このiPaDをアルツハイマー病モデルマウスに適用し、神経新生の活性化が病態改善につながるかを検証するとともに、その仕組みの解明にも挑みました。具体的には、iPaDをアルツハイマー病モデルマウスの海馬に導入し、神経新生、アミロイドβ蓄積、認知機能への影響を段階的に解析しました。
まず、iPaDを海馬に導入したアルツハイマー病モデルマウスでは、神経幹細胞の活性化と新しい神経細胞の産生が顕著に促進されました。神経幹細胞から生み出される未成熟な神経細胞(DCX陽性細胞[8])の数を指標として評価したところ、iPaDを導入した群では、これらの細胞数が対照群と比較して有意に増加しました。特に、iPaD導入後4週、8週、12週のいずれの時点においても増加が確認され、時間が経過しても効果が持続することが示されました(図1)。
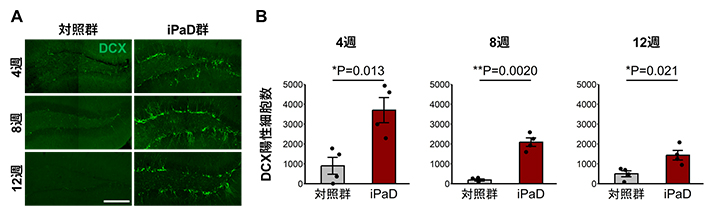
図1 iPaDによる神経新生の活性化
- A.5カ月齢のアルツハイマー病モデルマウス(神経新生の低下やアミロイドβの蓄積、認知機能低下が認められる時期)の海馬にiPaDを導入後、4週、8週、12週における未成熟な神経細胞(DCX陽性細胞)の代表的な画像(対照群およびiPaD群)。iPaD導入により、DCX陽性細胞(緑色に光っている細胞)の数が顕著に増加した。スケールバーは200マイクロメートル(μm、1μmは100万分の1メートル)。
- B.iPaD導入後4週、8週、12週におけるDCX陽性細胞数の定量結果(対照群およびiPaD群)。iPaD導入後、4週、8週、12週いずれの時点においても、DCX陽性細胞数は有意に増加した。統計的有意差:*P<0.05、**P<0.01。
次に、iPaDによる神経新生の活性化が、アルツハイマー病の主要な病理であるアミロイドβの蓄積にどのような影響を与えるかを検討しました。アミロイドβは脳内に蓄積することで神経細胞の機能を障害し、認知機能低下の原因となるタンパク質です。
iPaDを導入したマウスの海馬組織を解析した結果、アミロイドβプラーク[2]の面積は対照群と比較して有意に減少しました(図2A)。特に、iPaD導入後12週では、約50%の減少が認められ、統計的にも有意な差が確認されました(図2B)。この効果は、神経新生が活発に起こっている領域だけでなく、周辺領域においても認められました(図2A)。
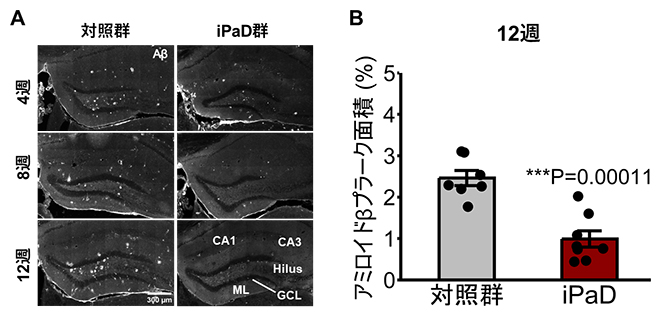
図2 iPaDによるアミロイドβの蓄積抑制
- A.5カ月齢のアルツハイマー病モデルマウスの海馬にiPaDを導入後、4週、8週、12週におけるアミロイドβプラークの代表的な画像(対照群およびiPaD群)。iPaD導入により、アミロイドβプラーク(点状に白く光っているところ)の蓄積が顕著に抑制された。
Aβ:アミロイドβ、CA1:海馬CA1領域、CA3:海馬CA3領域、Hilus:ヒルス領域(歯状回門)、GCL:顆粒細胞層(神経新生が活発に起こっている領域)、ML:分子層。スケールバー:300マイクロメートル(μm、1μmは100万分の1メートル)。 - B.iPaD導入後12週におけるアミロイドβプラーク面積の定量結果(対照群およびiPaD群)。iPaD導入後12週では、アミロイドβプラーク面積が約50%減少した。統計的有意差:***P<0.001。
従来の研究では、神経新生の促進だけではアミロイドβの蓄積を十分に抑制できないとされていましたが、本研究ではより強力な神経新生の活性化により、病理の改善が可能であることが示されました。
iPaDによる神経新生の活性化およびアミロイドβの減少が認知機能に与える影響を評価するため、空間記憶を測定するバーンズ迷路試験[9]をアルツハイマー病モデルマウスで実施しました。この試験では、マウスが複数の穴の中から記憶に基づいて正しい出口(ゴール)を見つけるまでの時間(到達時間)および移動距離を指標として解析しました。マウスの動きを追跡したところ、iPaD導入群は対照群と比較して効率よく目標地点に到達することを確認しました(図3A)。定量解析の結果、iPaD導入群では到達時間および移動距離がいずれも有意に短縮しました(図3B)。これらの結果から、iPaDによる神経新生の活性化は、空間記憶および学習能力の向上につながることが示されました。
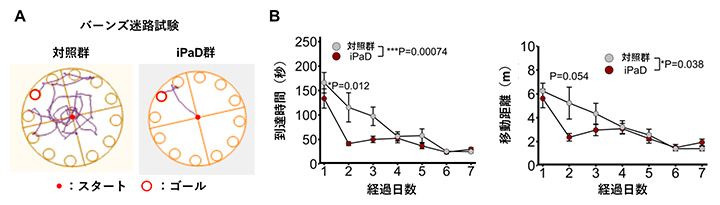
図3 iPaDによる認知機能の改善
- A.バーンズ迷路試験2日目におけるマウスの移動経路の代表例(対照群およびiPaD群)。iPaD導入群では、対照群と比較して効率的に目標地点(ゴール)へ到達することが確認された。
- B.目標地点(ゴール)までの到達時間および移動距離を定量した(対照群およびiPaD群)。試験期間中ゴールの穴は変えておらず、位置を覚えたマウスはほぼ最短時間・最小距離で到達できるようになる。到達時間、移動距離いずれの指標においても、対照群と比較してiPaD群で有意に短縮が認められた。統計的有意差:*P<0.05、**P<0.01、***P<0.001。
最後に、iPaDの作用メカニズムを明らかにするため、iPaD導入群と非導入群の脳で発現に差が生じた遺伝子を網羅的に調べました。その中で、iPaD導入群で発現が著しく低下していたPrkag2という遺伝子に着目しました。この遺伝子はアルツハイマー病患者およびアルツハイマー病モデルマウスで発現が増加しており、病態に関与している可能性が示唆されています。
そこで、レンチウイルスベクターを用いて、海馬においてPrkag2の遺伝子発現を抑制したところ、神経新生が有意に促進されました(図4A)。具体的には、未成熟な神経細胞であるDCX陽性細胞の数が増加し、その増加率は複数の候補遺伝子の中で最も高い結果となりました(図4B)。同時に、アミロイドβプラークの面積も有意に減少しました(図4C)。この効果は、iPaD導入群で発現が著しく低下していた他の遺伝子を抑制した場合にも一部認められましたが、Prkag2の抑制が最も強い効果を示しました(図4D)。
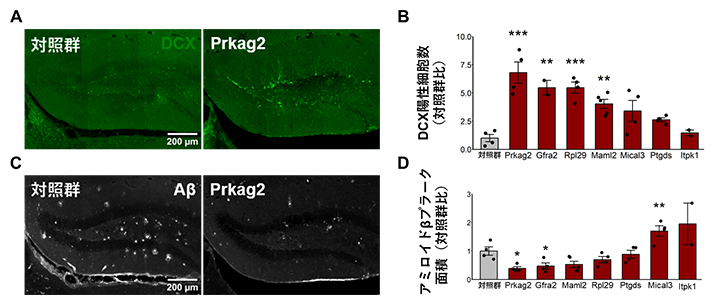
図4 Prkag2の抑制による神経新生の活性化およびアミロイドβの蓄積抑制
- A.Prkag2を抑制したアルツハイマー病モデルマウスの海馬における未成熟な神経細胞(DCX陽性細胞)の代表的な画像(対照群およびPrkag2抑制群)。Prkag2の抑制により、DCX陽性細胞の増加が確認された。
- B.Prkag2と同様にiPaD導入群で著しい発現低下を示した遺伝子Maml2、Ptgds、Gfra2、Rpl29、Itpk1、Mical3について、それぞれを抑制した実験を行った。DCX陽性細胞数を定量した結果、Prkag2の抑制によりDCX陽性細胞数が最も顕著に増加した。
- C.Prkag2を抑制したアルツハイマー病モデルマウスの海馬におけるアミロイドβプラークの代表的な画像(対照群およびPrkag2抑制群)。Prkag2の抑制により、アミロイドβプラークの減少が確認された。Aβ:アミロイドβ。
- D.Bと同様に各遺伝子の抑制実験を行った際のアミロイドβプラーク面積の定量結果。Prkag2の抑制により、アミロイドβプラーク面積は最も効果的に減少した。
統計的有意差:*P<0.05、**P<0.01、***P<0.001。
これらの結果から、Prkag2は神経新生とアミロイドβ蓄積の両方を制御する重要な因子であり、その抑制はアルツハイマー病の新たな治療戦略となる可能性が示されました。
- 注2)Kaise, T., Fukui, M., Sueda, R., Piao, W., Yamada, M., Kobayashi, T., Imayoshi, I., and Kageyama, R. (2022). Functional rejuvenation of aged neural stem cells by Plagl2 and anti-Dyrk1a activity. Genes Dev. 36, 23-37.
今後の期待
本研究により、iPaDにより神経新生を強力に活性化することで、アルツハイマー病の主要な病理であるアミロイドβの蓄積を抑制し、さらに認知機能の改善につながることが明らかになりました。特に、神経幹細胞の機能を維持しながら神経新生を持続的に活性化できる点は、従来の手法にはない大きな特長です。また、Prkag2の抑制によってもiPaDと同様の効果が得られたことから、Prkag2抑制のアルツハイマー病治療への応用も期待されます。今後は、本手法の安全性や長期的な効果を検証するとともに、ヒトへの応用に向けた研究を進めることで、アルツハイマー病をはじめとする神経変性疾患の新たな治療法の開発につながることが期待されます。
補足説明
- 1.神経幹細胞
神経細胞やグリア細胞へと分化する能力を持つ細胞。成体脳では休眠状態にあるが、特定の刺激により活性化し増殖・分化する。 - 2.アルツハイマー病、アミロイドβ、アミロイドβプラーク
アルツハイマー病(アルツハイマー型認知症)は、認知症の原因疾患で最も多い神経変性疾患。アミロイドβはアルツハイマー病の原因物質の一つとされるタンパク質であり、脳内に蓄積し神経細胞の機能障害や細胞死を引き起こす。アミロイドβが凝集して形成される塊はアミロイドβプラークと呼ばれ、老齢期やアルツハイマー病患者の脳に特徴的に見られる病理構造である。 - 3.神経新生
脳内で新しい神経細胞が生まれる現象。主に海馬([6]参照)で起こり、学習や記憶などの認知機能に関与する。加齢や疾患により低下することが知られている。 - 4.iPaD
影山チームディレクターらが2022年に発表した、特定の遺伝子(Plagl2の誘導とDyrk1aの抑制)を組み合わせて神経幹細胞を活性化する手法。加齢により低下した神経幹細胞の機能を回復させることを目的とする。iPaDはinducing Plagl2 and anti-Dyrk1aの略。 - 5.Prkag2
細胞内のエネルギー状態を調節する酵素複合体に関与する遺伝子。アルツハイマー病患者およびアルツハイマー病モデルマウスにおいて発現が上昇することが報告されている。Prkag2はprotein kinase AMP-activated non-catalytic subunit gamma 2の略。 - 6.海馬
脳の内側に位置する領域であり、記憶の形成や空間認知に重要な役割を果たす。神経新生が生涯にわたり起こる数少ない部位の一つ。 - 7.レンチウイルス
遺伝子を細胞内に導入するために用いられるウイルスベクター。目的の遺伝子を特定の細胞に効率よく導入できる。 - 8.DCX陽性細胞
DCX(doublecortin:ダブルコルチン)は発生中の中枢神経や末梢神経でつくられるタンパク質であり、未成熟な神経細胞の指標となる。DCX陽性細胞は神経新生の程度を評価する際に広く用いられる。 - 9.バーンズ迷路試験
マウスの空間記憶や学習能力を評価する行動試験である。複数の穴の中から正しい出口(ゴール)を見つける能力を測定する。
国際共同研究グループ
理化学研究所 生命機能科学研究センター 神経幹細胞研究チーム
チームディレクター 影山 龍一郎(カゲヤマ・リョウイチロウ)
リサーチ・アソシエイト 福井 雅弘(フクイ・マサヒロ)
研究パートタイマーⅠ(研究当時、現 客員研究員)正木 大夢(マサキ・タイム)
(京都大学 大学院医学研究科 大学院生(研究当時))
マサチューセッツ工科大学(米国)
研究員 貝瀬 峻(カイセ・タカシ)
スタンフォード大学(米国)医学部
大学院生 坂本 泰良(サカモト・タイラ:Tyler Sakamoto)
研究支援
本研究は、理化学研究所運営費交付金(脳神経科学研究、生命機能科学研究)で実施し、日本医療研究開発機構(AMED)革新的先端研究開発支援事業(AMED-CREST)「成体脳神経幹細胞の機能低下メカニズムの解明と再活性化に向けた技術開発(研究代表者:影山龍一郎)」、日本学術振興会(JSPS)科学研究費助成事業特別推進研究「短周期振動する遺伝子発現の生理学的意義について(研究代表者:影山龍一郎、JP21H04976)」による助成を受けて行われました。
原論文情報
- Masahiro Fukui, Takashi Kaise, Taimu Masaki, Tyler Sakamoto, and Ryoichiro Kageyama, "Activation of neurogenesis improves amyloid-β pathology and cognitive function through AMP kinase signaling in Alzheimer's disease model mice", Cell Reports, 10.1016/j.celrep.2026.117250
発表者
理化学研究所
生命機能科学研究センター 神経幹細胞研究チーム
リサーチ・アソシエイト 福井 雅弘(フクイ・マサヒロ)
チームディレクター 影山 龍一郎(カゲヤマ・リョウイチロウ)
 影山 龍一郎
影山 龍一郎
 福井 雅弘
福井 雅弘
発表者のコメント
今回の研究では、神経幹細胞の機能を回復させることで、認知機能を改善できる可能性を示すことができました。実験を進める中で、神経新生の活性化がアミロイドβの減少にもつながるという結果が得られたときは、大きな驚きとともに強い手応えを感じました。(福井 雅弘)
今後、今回の発見を核酸医薬の開発につなげていきたいです。(影山 龍一郎)
報道担当
理化学研究所 広報部 報道担当
お問い合わせフォーム
